Санкт-Петербург, 2002 г.
РАЗДЕЛ 7. ИЗБИРАТЕЛЬНАЯ ТОКСИЧНОСТЬ
ГЛАВА 7.3.
Пульмонотоксичность
Пульмонотоксичность - это свойство химических веществ, действуя на организм немеханическим путем вызывать структурно-функциональные нарушения со стороны органов дыхания.
Обладая огромной площадью поверхности, лёгкие находятся в состоянии постоянного воздействия ксенобиотиков, содержащихся во вдыхаемом воздухе. В подавляющем большинстве случаев, когда концентрации веществ малы, такие воздействия никак не проявляют себя. Если же уровень воздействия достаточно высок, формируется токсический процесс, тяжесть которого колеблется в широких пределах от незначительных явлений раздражения (транзиторная токсическая реакция) до тяжелейших расстройств со стороны многих органов и систем (интоксикация). Пульмонотоксичность может проявляться как при местном, так и при резорбтивном действии токсикантов. Более того, не все вещества, действующие ингаляционно, обладают пульмонотоксичностью. Для многих токсикантов легкие лишь входные ворота, которые они проходят, не вызывая повреждений (монооксид углерода, мыщьяковистый водород, стибин, ТЭС и т.д.). Вместе с тем к некоторым соединениям, проникающим в организм и другими путями (например, через желудочно-кишечный тракт) ткань легких чрезвычайно чувствительна. Вещества, порог чувствительности к которым органов дыхания существенно ниже, чем других органов и систем, и клиника поражения которыми характеризуется нарушениями со стороны, прежде всего, органов дыхания, условно можно отнести к группе пульмонотоксикантов.
Как следует из определения, не все вещества, вызывающие нарушения со стороны дыхательной системы обладают пульмонотоксичностью. Так, ксенобиотики, вмешивающиеся в механизмы центральной регуляции дыхания (наркотические аналгетики, неэлектролиты, барбитураты и др.), отравление которыми сопровождаются выраженными функциональными нарушениями со стороны дыхательной системы, к числу пульмонотоксикантов в строгом смысле слова не относятся.
По большей части пульмонотоксичность проявляется при ингаляционном способе воздействия ксенобиотиков в форме газов, паров и аэрозолей. Перечень веществ, действующих на организм ингаляционно, очень велик и включает загрязнители атмосферного воздуха и воздуха рабочей зоны, гербициды, пестициды, сильнодействующие и ядовитые вещества (СДЯВ - при нештатных ситуациях на производствах), отравляющие вещества (ОВ - в ходе военных конфликтов) и т.д.
Некоторые вещества вызывают поражение уже вследствие однократного воздействия, другие провоцируют патологию только при длительной экспозиции или повторных воздействиях.
Каким бы образом не формировался токсический процесс, клинические эффекты группируются вокруг достаточно ограниченного числа типических патологических состояний. К их числу относятся: явления обратимого раздражения верхнего и нижнего отделов дыхательных путей; стойкое поражение дыхательных путей; повреждение терминальных респираторных единиц легких (ацинусов) в форме воспалительных, пролиферативных процессов и нарушения проницаемости альвеолярно-капиллярного барьера; новообразования. Некоторые токсиканты способны вызывать множественные нарушения со стороны дыхательной системы. Так, асбест вызывает не только фиброз легочной ткани, но и рак легких. Сигаретный дым вызывает самый широкий спектр патологических состояний от хронического бронхита до эмфиземы и рака легких.
1. Краткая характеристика морфологии дыхательной системы
Выделяют три основных отдела дыхательной системы: назофарингиальный (полость носа, ротовая полость, гортань), трахеобронхиальный (трахея, первичные бронхи, вторичные бронхи), лёгочный (терминальные бронхи, респираторные бронхиолы, альвеолярные ходы, альвеолярные мешочки, альвеолы). Газообмен осуществляется в структурах, располагающихся ниже респираторных бронхиол (ацинус). В тканях лёгких и бронхов обнаружено более 40 типов клеток, каждый из которых обладает существенными морфо-функциональными особенностями и, следовательно, особой чувствительностью к действию токсикантов.
1.1. Назофарингиальный отдел
Назофарингиальная область дыхательной системы человека начинается в носовых ходах, продолжается горизонтально, изгибается, под углом 900, постепенно переходит в фаринголарингиальный отдел. Анатомический изгиб дыхательных путей образует первый барьер на пути ингалируемых токсикантов. Здесь вдыхаемые частицы аэрозоля диаметром 5 - 10 мкм сталкиваются со стенками воздухоносных путей и оседают на выстилающем их эпителии. Область гортани является анатомическим продолжением назофарингиальной области, её поражение отмечается при аналогичных условиях.
1.2. Трахеобронхиальный отдел
Этот отдел воздухоносных путей является вторым эшелоном защиты лёгких от токсикантов. Дыхательные пути покрыты реснитчатым эпителием. Секреторные клетки, бокаловидные клетки, щеточные клетки, клетки Клара и целый ряд других клеток продуцируют секрет, тонким слоем выстилающий слизистую дыхательных путей. Реснички эпителия совершают ритмические движения, поддерживая ток слизи из легких. С этим током из лёгких и дыхательных путей выводятся адсорбировавшиеся на поверхности эпителия частицы веществ не растворяющихся в воде (и, следовательно, секрете трахеобронхиальных желез). Скорость движения частиц по поверхности эпителия трахеи и бронхов составляет 1 - 4 мкм/ мин. Мукоцилиарный транспорт - важнейший механизм освобождения дыхательных путей от ингалированных частиц аэрозолей.
Дыхательные пути подразделяются на три основные категории: бронхи, содержащие хрящ, респираторные бронхиолы, участвующие в газообмене, альвеолярные ходы. Хрящесодержащие бронхи выполняют функцию своеобразного каркаса лёгких и совместно с вышележащими дыхательными путями образуют так называемое "мёртвое пространство", объём которого оценивается физиологическими методами.
Респираторные бронхиолы представляют собой короткие трубочки диаметром около 0,5 мм с эластичной стенкой. Их поверхность выстлана реснитчатым и кубовидным эпителием, который постепенно уплощаясь, превращается в альвеолярный эпителий, выстилающий альвеолярные ходы, альвеолярные мешочки, альвеолы.
1.3. Паренхима легких
Паренхима лёгких образована огромным количеством альвеол. Альвеолы представляют собой тонкостенные микроскопические полости, открывающиеся в альвеолярный мешочек, альвеолярный ход или непосредственно в респираторную бронхиолу. Несколько сотен тесно примыкающих друг к другу альвеолярных ходов и мешочков образуют терминальную респираторную единицу (ацинус).
Газообмен, в основном, осуществляется в альвеолах. Барьер на пути диффундирующих газов образуют мембраны, состоящие из слоя альвеолярного эпителия, промежуточного вещества и эндотелиальных клеток капилляров. Альвеолярный эпителий образуется клетками трёх типов. Клетки первого типа представляют собой сильно уплощенные структуры, выстилающие полость альвеолы. Именно через эти клетки осуществляется диффузия газов. Клетки второго типа имеют кубовидную форму. Их поверхность покрыта микроворсинками, а цитоплазма богата ламеллярными телами. Эти клетки депонируют сурфактант - поверхностно-активное вещество сложной липопротеидной природы, содержащееся в тонкой пленке жидкости, выстилающей внутреннюю поверхность альвеол. Сурфактант регулирует силу поверхностного натяжения альвеолярной мембраны. Уменьшая силу поверхностного натяжения стенок альвеол, вещество не позволяет им спадаться. Его содержание контролируется процессами синтеза, выделения и депонирования. Клетки третьего типа, это легочные макрофаги, фагоцитирующие чужеродные частицы, попавшие в альвеолы, и участвующие в формировании иммунологических реакций в лёгочной ткани. Макрофаги способны к миграции по дыхательным путям, лимфатическим и кровеносным сосудам.
Интерстициальное вещество обычно представлено несколькими эластическими и коллагеновыми волокнами, фибробластами, иногда клетками других типов.
При патологических процессах с вовлечением любого компонента терминальной респираторной единицы - эпителия, эндотелия, интерстиция, затрудняется газообмен в лёгких. Денудация эпителия приводит к нарушению синтеза, выделения и депонирования сурфактанта, проницаемости альвеолярно-капиллярного барьера, экссудации отечной жидкости в просвет альвеолы; интерстициальный фиброз затрудняет диффузию газов; повреждение эндотелия усиливает проницаемость альвеолярно-капиллярного барьера, вызывает гемодинамические нарушения в легких, изменяет нормальное соотношение объема вентиляции и гемоперфузии легких и т.д.
1.4. Циркуляция крови и лимфы в лёгких
Кровеносные сосуды в лёгких располагаются параллельно воздухоносным путям. Сосуды, питающие бронхи, обеспечивают кровоснабжение до уровня терминальных бронхиол. Они ответвляются непосредственно от аорты и межреберных артерий. Венозная кровь от трахеи и бронхов оттекает по бронхиальным венам и собирается в vv. azygos и hemiazygos. В паренхиме лёгких бронхиальные сосуды образуют анастомозы с лёгочными венулами.
Лёгочные артерии обеспечивают транспорт бедной кислородом крови к терминальным респираторным единицам. Они входят в лёгочную ткань, примыкая к основным бронхам, и движутся, разветвляясь, параллельно разветвлению бронхиального дерева. Венозная кровь, богатая кислородом, оттекает по легочным венам тем же путём. В области терминальных респираторных единиц лёгочные артерии разветвляются, давая начало сосудам, кровоснабжающим ацинус. Легочные вены дренируют кровь, оттекающую от нескольких ацинусов.
Капиллярная сеть в лёгких чрезвычайно развита и имеет большой суммарный объём. Скорость кровотока в ней минимальна, что создаёт условия для газообмена между протекающей кровью и альвеолярным воздухом. Капиллярная сеть обнимает несколько альвеол. Протекающая по ним кровь собирается в венулы.
Объём лёгочной ткани регулируется системой лимфатических сосудов. Лимфатические сосуды представлены капиллярами, локализующимися в соединительной ткани лёгких, и коллекторными лимфатическими сосудами. Различают глубокую и поверхностную системы лимфатических сосудов, связанных между собой. Развитая лимфатическая система дренирует лёгочную ткань, неся лимфу к лимфатическим узлам, расположенным в области корня лёгкого. Помимо лимфатических узлов, по ходу бронхов, обнаруживаются участки лимфоидной ткани. Эта так называемая бронхоассоциированная лимфоидная ткань (БАЛТ) играет важную роль в формировании иммунных реакций организма.
В лимфатических узлах и БАЛТ накапливаются частицы нерастворимого в воде аэрозоля, попавшего в легкие и не выделившиеся с помощью мукоцилиарного тока. Эти частицы захватываются макрофагами, мигрирующими по лимфатическим сосудам в лимфоидную ткань.
2. Физиология дыхательной системы
С точки зрения токсиколога интерес представляют три аспекта физиологии дыхательной системы. Это вентиляция, газообмен, метаболизм ксенобиотиков и биологически активных веществ.
2.1. Вентиляция
Вентиляция лёгких - это совокупность физиологических актов, направленных на продвижение воздуха по воздухоносным путям к терминальным респираторным единицам (ацинусам), где и осуществляется газообмен. Способность к вентиляции определяется механическими факторами, такими как подвижность грудной клетки и диафрагмы, проходимость воздухоносных путей, а также эластичностью легочной ткани.
Патологические процессы, развивающиеся в лёгких в ходе токсического процесса, могут вызвать три типа изменений процесса вентиляции:
- структурно-механические. Состояния, сопряженные со снижением способности осуществлять полный акт вдох-выдох. Они наблюдаются при нарушении функций нервно-мышечного (слабость, паралич дыхательной мускулатуры) и опорного аппарата, ответственного за внешнее дыхание (интоксикации ФОС, карбаматами, ботулотоксином, тетродотоксином, миорелаксантами и т.д.). Этот тип нарушений распознаётся при проведении ряда дыхательных тестов, и обозначается как "рестриктивный".
- повреждающие дыхательные пути. Повреждение дыхательных путей в форме острой (химический ожег, интоксикация ипритом, люизитом и т.д.) или хронической (длительное воздействие поллютантов, курение) воспалительной реакции, а также бронхоспастические состояния существенно затрудняют выдох (интоксикация ФОС, карбаматами и др). Этот тип нарушений обозначается как "обструктивный".
- нарушающие эластичность легочной ткани. Усиление ригидности лёгочной ткани, наблюдающееся при фиброзе (острая интоксикация паракватом), сопровождается существенным снижением легочного объёма. Противоположное состояние, наблюдаемое при эмфиземе, которая приводит к снижению ригидности лёгочной ткани, но сопряжена с затруднением движения воздуха по дыхательным путям.
2.1.1. Легочные объемы
Максимальное количество воздуха, содержащегося в лёгких и дыхательных путях человека, которое может быть заменено на воздух окружающей среды при совершении максимального вдоха и выдоха, называется жизненной ёмкостью лёгких (ЖЁЛ) (рисунок 1). Даже при максимально возможном выдохе лёгкие полностью не спадаются, следовательно, небольшой объём воздуха задерживается в них. Этот объём воздуха называется остаточный объём (ОО). Сумма ЖЁЛ и ОО называется общей лёгочной ёмкостью (ОЛЁ). В состоянии покоя количество воздуха, участвующего в актах вдох-выдох (дыхательный объём - ДО), составляет лишь незначительную часть ЖЁЛ. Воздух остающийся в лёгких после обычного выдоха составляет функциональную остаточную ёмкость (ФОЁ). В условиях, требующих усиления вентиляции, возможны два пути: увеличение дыхательного объёма и учащение дыхания.
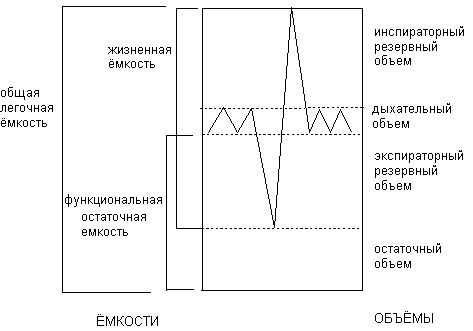
Рисунок 1. Жизненные ёмкости и объемы легких
При развитии токсических процессов развиваются патологические состояния, сопровождающиеся изменением легочных объёмов и ёмкостей. Например, лёгочные объёмы и ёмкости могут существенно возрастать при астме и хронических обструктивных заболеваниях, сопровождающихся эмфиземой. В этих условиях существенно возрастает ОЛЁ главным образом за счет значительного увеличения ОО и ФОЁ. Напротив, состояния связанные с повышением ригидности лёгочной ткани (фиброз, гранулематоз лёгких) сопровождаются снижением ОЛЁ и других объёмов и ёмкостей лёгких. Следствием этих изменений является ухудшение вентиляции ацинусов. И в том и в другом случае существенно снижаются резервные возможности внешнего дыхания, и в случае необходимости усилить вентиляцию (физическая нагрузка), сделать это не представляется возможным.
2.1.2. Рефлексы, влияющие на дыхание
Рефлексы верхних дыхательных путей. В 1870 Кречмер описал рефлекс, формирующийся при раздражении (в том числе химическими веществами, например, аммиаком) верхних дыхательных путей. Проводниками сигнала являются обонятельный, тройничный и языкоглоточный нервы. Раздражение окончаний нервов приводят к немедленной реакции проявляющейся апное, брадикардией, падением, а затем подъёмом артенриального давления. Аллен, в 1928 году показал наличие этого рефлекса у человека.
Рефлексы глубоких дыхательных путей. Раздражение нервных окончаний глубоких дыхательных путей инициирует кашель. Наличие этого рефлекса при ингаляции токсикантов у человека описано Салем и Авиадо в 1974 году.
Бронхоальвеолярные рефлексы. В 1868 году Герингом и Брейером описан рефлекс, регулирующий глубину и частоту дыхания. Проводником рефлекса является блуждающий нерв. Нервные окончания, залегающие в легочной ткани, раздражаются при ее растяжении. Поток нервных импульсов в дыхательный центр служит сигналом для прерывания акта вдоха и инициации выдоха. Спадение легочной ткани приводит к прекращению импульсации и возобновлению вдоха. При раздражении нервных окончаний (отечной жидкостью при отеке легких) акт вдоха прерывается раньше, чем в норме. Это приводит к учащенному, поверхностному дыханию.
Краткая характеристика рефлексов, лежащих в основе реакций внешнего дыхания, на возможные токсические воздействия представлена в таблице 1.
Таблица 1. Рефлексы дыхательной системы
Локализация рецепторов (краниальные нервы) |
Физиологические и химические стимулы |
Реакция дыхательной и сердечно-сосудистой систем |
Верхние дыхательные пути (I, V, X) |
Газы, пары, аэрозоли ирритантов |
Апное, брадикардия, спазм сосудов |
Глубокие дыхательные пути |
Газы, пары, аэрозоли ирритантов |
Кашель |
Бронхоальвеолярные рецепторы: (X) медленно адаптирующиеся (X) быстро адаптирующиеся |
Умеренная воспалительная реакция Ателектаз; выраженная воспалительная реакция |
Апное Тахипное |
Кардиопульмональные рецепторы: (Х) легочные вены (Х) левый желудочек |
Понижение АД Повышение АД; алкалоиды группы вератрина |
Апное Брадикардия, расширение сосудов |
Барорецепторы: (Х) дуга аорты (IX) каротидный клубочек |
Понижение АД Понижение АД |
Апное, брадикардия, расширение сосудов Апное, брадикардия, расширение сосудов |
Хеморецепторы: (Х) дуга аорты (IX) каротидный клубочек |
Гипоксия; цианиды Гипоксия; цианиды |
Тахипное, тахикардия, расширение сосудов Тахипное, тахикардия, расширение сосудов |
Соматические рецепторы: Болевые рецепторы Мышечные рецепторы Висцеральные рецепторы |
Воспаление; алгогены, ирританты Физическая работа Сдавление |
Тахипное Тахипное Тахипное |
(D.M. Aviado, H. Salem, 1987)
2.1.3. Механизмы регуляции тонуса бронхов
Тонус гладкомышечных волокон бронхов определяет диаметр последних. Бронходилятация наблюдается при активации
Ингаляция пыли, а у сенсибилизированных людей, целого ряда других веществ (см. ниже) может приводить к выраженному бронхоспазму. Причина явления - высвобождение в легочной ткани бронхоспастических аутокоидов. Тучные клетки и лейкоциты высвобождают гистамин, серотонин, аденозин, факторы агрегации тромбоцитов (ФАТ) и другие биологически активные вещества, вызывающие спазм гладкой мускулатуры бронхов. Бронхоспазм вызывают также вещества, активирующие холинергическую иннервацию дыхательных путей (ФОС, карбаматы). Механизмы регуляции тонуса бронхов представлены в таблице 2.
Таблица 2. Механизмы регуляции тонуса бронхов
Эффект |
Механизмы |
Бронхоспазм |
Рефлекс раздражения верхних дыхательных путей |
Рефлекс раздражения глубоких дыхательных путей |
|
Кардиопульмональный рефлекс |
|
Возбуждение барорецепторов аортальной дуги и каротидного клубочка |
|
Возбуждение блуждающего нерва |
|
Активация холинэргических рецепторов |
|
Активация серотонинэргических рецепторов |
|
Активация гистаминэргических рецепторов |
|
Активация пуринэргических рецепторов |
|
Расширение бронхов |
Возбуждение симпатической иннервации |
Активация адренэргических рецепторов |
|
Возбуждение хеморецепторов аортальной дуги и каротидного клубочка |
|
Выброс адреналина надпочечниками |
|
Мышечная активность |
2.2. Газообмен
Газообмен осуществляется в ацинусах легких. Упрощенно суть процесса состоит в диффузии кислорода из альвеолярного воздуха в кровь и диоксида углерода из крови в альвеолярный воздух. Движущей силой процесса является разница парциальных давлений газов в крови и альвеолярном воздухе (рисунок 2).
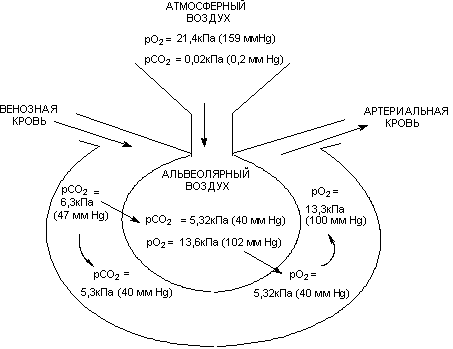
Рисунок 2. Процесс газообмена между воздухом и кровью
Как уже указывалось, диффузия осуществляется через трёхслойную мембрану, образованную альвеолярным эпителием, интерстициальной тканью и эндотелием капилляров. Поступивший в кровь кислород растворяется в плазме, проникает через мембрану эритроцитов и образует обратимый комплекс с гемоглобином. Нарушение диффузии возможно при повреждении любого из биологических слоёв, образующих альвеолярно-капиллярный барьер. Классическими примерами состояний этого типа являются токсический отёк лёгких (хлор, оксиды азота, фосген и др.), фиброз лёгких (паракват), диффузное замещение плоского альвеолярного эпителия кубовидным вследствие хронической ингаляции ряда ксенобиотиков (курение).
Нарушение газообмена может стать результатом изменения необходимого соотношения между объёмом вентиляции лёгких и их кровоснабжения, что наблюдается в частности при эмфиземе.
Таким образом, изменения газообмена обусловлены заболеваниями легких, развивающимися как по рестриктивному, так и по обструктивному или смешанному типу.
Физиологическими следствиями нарушения газообмена являются:
- учащение дыхания и увеличение дыхательного объёма;
- гипоксия в покое или при нагрузке;
- ограничение возможности выполнения физических нагрузок.
При токсическом отеке легких нарушение газообмена является основной причиной развития состояний, угрожающих жизни пострадавшего, а иногда и гибели.
Для оценки диффузионной способности легких необходимо знать количество газа, проникающего через альвеолярно-капилярный барьер в единицу времени при определённом градиенте парциального давления газа в альвеолах и крови. Для оценки состояния легких часто используют метод однократного вдоха или пролонгированной ингаляции монооксида углерода. СО прочно связывается с гемоглобином и при определенном содержании в окружающем воздухе образует вполне определенное количество карбоксигемоглобина. Оценивая уровень карбоксигемоглобинемии при ингаляции СО в фиксированной концентрации можно судить о диффузионной способности легких.
Другим методом оценки диффузионной способности легких является изучение газового состава артериальной крови в покое и при физической нагрузке. В случае корректного выполнения исследований это наиболее чувствительный индикатор состояния дыхательной системы.
2.3. Метаболизм ксенобиотиков и биологически активных веществ
Помимо осуществления внешнего дыхания респираторная система имеет и ряд других важных функций. Среди них: продукция и секреция гормонов и медиаторов, биотрансформация и выведение из организма ксенобиотиков и некоторых биологически активных веществ. В частности в лёгких активно метаболизируют основные амины, полициклические ароматические углеводороды. Ферментные системы, ответственные за метаболизм, те же, что и в других органах. Это, прежде всего, оксидазы смешанной функции (монооксигеназы, цитохром-Р450-зависимые оксидазы) и несколько коньюгирующих энзимов, включая глюкуронозилтрансферазу, сульфотрансферазу, глютатионтрансферазу. В сравнении с печенью напряженность процессов биотрансформации в лёгких значительно ниже. Так, содержание цитохрома-Р-450 в легких составляет 10 - 20% от уровня, определяемого в печени. Основные клеточные структуры, ответственные за метаболизм ксенобиотиков - пневматоциты 2-го порядка.
При анализе токсичности необходимо учитывать способность лёгких к селективному захвату ряда веществ (прежде всего органических аминов). Так, активно захватывается лёгкими паракват, превращаясь затем в пульмонотоксикант. В качестве примера биологически активных веществ, метаболизируемых в лёгких, можно привести полипептид ангиотензин-1, трансформируемый в лёгких в ангиотензин-11. Энзим, катализирующий это превращение, обнаружен в эндотелии лёгочных капилляров. Превращение серотонина (МАО), некоторых простогландинов, также происходит в основном в лёгких. Таким образом, повреждение легочной ткани может иметь целый спектр последствий, влияющих на функциональное состояние организма в целом.
2.4. Депонирование и клиаренс ксенобиотиков в легких
Ксенобиотики попадают в легкие в форме газов и аэрозолей. Их дальнейшая судьба зависит, в основном, от свойств и агрегатного состояния и может схематически быть представлена следующим образом (рисунок 3).
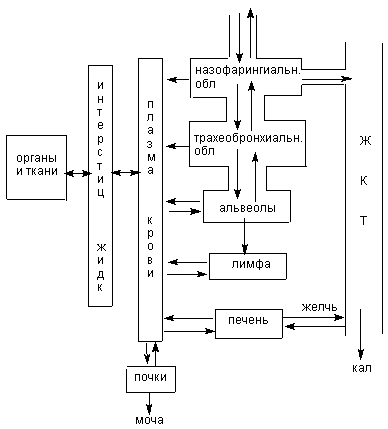
Рисунок 3. Схема движения ксенобиотика (депонирование и клиаренс) в организме при ингаляционном поступлении
Сайт депонирования ингалируемых газов определяется степенью их растворимости в тонком слое жидкости, выстилающей слизистую дыхательных путей и альвеолярный эпителий. Хорошо растворимые в воде вещества, например аммиак, диоксид серы преимущественно фиксируются верхним отделом дыхательных путей. По этой причине основной токсический эффект этих ксенобиотиков реализуется в верхних дыхательных путях, а ниже лежащие отделы поражаются лишь при очень высоких концентрациях. Напротив, плохо растворимые в воде вещества, такие как фосген, оксиды азота преимущественно поражают глубокие отделы лёгких. То есть, чем менее растворим газ в воде, тем выше его потенциал в плане поражения паренхимы легких. Водо-растворимые вещества достигают глубоких отделов легких при дыхании через рот, что наблюдается при физической нагрузке, либо когда человек находится в бессознательном состоянии. В обоих случаях степень поражения паренхимы лёгких токсикантами, при прочих равных условиях, увеличивается.
На депонирование частиц в лёгких оказывают влияние различные факторы. Среди них: анатомические особенности дыхательной системы (см. выше), характеристика аэрозоля, характер дыхания. Решающим фактором является размер частиц. Частицы диаметром более 50 мкм практически не проникают в дыхательные пути, до 10 мкм - оседают преимущественно в носоглотке (более 80%), 0,5 - 3 мкм - преимущественно в глубоких дыхательных путях и альвеолах (около 80%). Более мелкие частицы, как правило, не задерживаются в лёгких (минимальная задержка отмечается при диаметре частиц 0,25 - 0,30 мкм). Высокодисперсные аэрозоли (диаметр частиц менее 0,1 мкм) ведут себя практически как газы.
Клиаренс частиц оказывается определяющим в токсических эффектах ингалируемых агентов. Под клиаренсом в данном случае понимают элиминацию частиц из организма или перемещение их в другие органы после первичного депонирования в дыхательных путях. В целом, частицы, хорошо растворимых в воде веществ, и газы абсорбируются эпителиальным слоем и затем проникают в кровь. Клиаренс нерастворимых веществ зависит от того, где абсорбированы частицы. Если максимум абсорбции осуществляется в носоглотке и крупных воздухоносных путях, эпителий которых имеет микроворсинки (см. выше), частицы удаляются с помощью восходящего мукоцилиарного тока в полость рта, откуда поступают в желудочно-кишечный тракт. На уровне альвеол, где цилиарный эпителий отсутствует, клиаренс частиц осуществляется макрофагами. Эти клетки ответственны за удаление и нейтрализацию частиц, попадающих в дыхательные пути. Они захватывают аэрозоль, а затем мигрируют в лимфатическую систему или к верхним дыхательным путям. Вследствие этого любое вещество, влияющее на количество макрофагов в лёгких или их функциональную активность, изменяет чувствительность дыхательной системы к патогенным факторам. Этапы взаимодействия макрофагов с частицами, следующие: хемотаксис, адгезия частиц к фагоциту, фагоцитоз частиц, образование первичных лизосом, слияние их со вторичными лизосомами, разрушение частиц. Повреждение защитных механизмов легких возможно при повреждении токсикантом любого из этих этапов. Многие ксенобиотики вызывают изменение числа макрофагов в лёгких и их свойств (таблица 3).
Таблица 3. Вещества, влияющие на количество и качественные характеристики макрофагов в легких
Снижают количество макрофагов |
Повышают количество макрофагов |
Подавляют фагоцитарную активность макрофагов |
Оксид свинца, Хлорид никеля, Оксид никеля, Хлорид кадмия, Монооксид углерода, Кристаллы кварца, Табачный дым, Пыль. |
Кремний, Асбест, Кадмий, Акролеин, Диоксид Марганца, Сурьма, Озон, Оксиды азота |
Кадмий, Никель, Медь, Ртуть, Цинк, Платина, Ванадий. |
Степень поражения макрофагов также определяется химическим составом, размерами, формой ингалируемых частиц. Судьба макрофага зависит от его способности разрушить фагоцитированную частицу. В случае неспособности выполнить эту задачу, фагоцит, как правило, гибнет. Гибель макрофагов приводит к выходу в лёгочную ткань лизосомальных энзимов, простогландинов, коллагеназы, эластазы, плазмин-активирующих факторов и других биологически активных веществ, что инициирует воспалительный процесс в легких, фиброз, эмфизему, гранулематоз и т.д.
Продукция интерферона макрофагами угнетается озоном и оксидами азота.
Важную роль в удалении частиц из лёгких играют также нейтрофилы, особенно в период формирования воспалительного процесса. Наконец, некоторое количество частиц, попавших в альвеолы, может проникать в кровеносные и лимфатические сосуды без посредников.
3. Основные формы патологии дыхательной системы химической этиологии
Поражение органов внешнего дыхания токсикантами может быть следствием непосредственного их действия в форме газов и аэрозолей на дыхательную систему (подавляющее большинство токсичных агентов), либо накопления ксенобиотиков или продуктов их метаболизма в легочной ткани, проникших в организм другими путями (бензин, хлорированные углеводороды, паракват и т.д.).
Острые отравления веществами, действующими непосредственно или опосредованно на органы дыхания, сопровождаются рядом респираторных синдромов, среди которых основные: острый ларингит и трахеобронхит, отек лёгких, острая диффузная интерстициальная пневмония, острая дыхательная недостаточность.
Последствиями подострых воздействий, а также результатом длительного контакта с токсикантами могут стать: длительно текущие воспалительные процессы дыхательных путей (риниты, синуситы, трахеобронхиты, бронхоэктатическая болезнь), эмфизема, облитерация верхних дыхательных путей, гиперреактивные состояния дыхательных путей, в том числе бронхиальная астма, хронические аллергические альвеолиты, интерстициальный фиброз, пневмокониоз, новообразования и др.
3.1. Острые ингаляционные поражения
Многие газы и аэрозоли вызывают острые токсические процессы в дыхательной системе. В основе этих процессов лежат либо гиперактивация физиологических защитных реакций организма на действие чужеродных веществ, либо альтерация легочной ткани.
Немедленные реакции организма на действие токсикантов изучены достаточно хорошо. Прежде всего, это кашель, секреция слизи, бронхоспазм, умеренный отек дыхательных путей - защитные реакции на вредные воздействия. При интенсивных воздействиях такие транзиторные токсические реакции перерастают в тяжелые патологические состояния.
Афферентные нервы в дыхательных путях, участвующие в кашлевом рефлексе, стимулируются либо непосредственно путем раздражения токсикантом нервных окончаний либо опосредованно, путем инициируемого ксенобиотиком высвобождения в тканях биомедиаторов, таких как гистамин, простогландины и др. Кашель способны вызывать все вещества, обладающие раздражающим действием на слизистые дыхательных путей (см. "Раздражающее действие"). Чрезмерный по выраженности или продолжительности кашель может стать причиной серьёзных дисфункций особенно у чувствительных к токсикантам лиц. Ингаляция токсиканта в концентрациях, не вызывающих вредного действия у здорового человека, может у чувствительного лица сопровождаться тяжелым, выводящим из строя кашлем. Причиной повышенной чувствительности нередко бывает предшествующий контакт с веществом.
Стимуляция выделения слизи подслизистыми железами дыхательных путей и бокаловидными клетками - еще одна защитная реакция на ксенобиотик, которая может перерасти в патологическое состояние. Даже легкие формы ингаляционного отравления ФОС сопровождаются выраженной гиперсекрецией бронхиальных желез, существенно затрудняющей дыхание (бронхорея). Гипертрофия слизистых желез и гиперплазия бокаловидных клеток отмечаются при экспериментальном воздействии на лабораторных животных ряда промышленных токсикантов, например диоксида серы. Так называемая "доброкачественная гиперсекреция" или профессиональный бронхит - типичное состояние у лиц, профессионально контактирующих с раздражающими веществами, дымами, парами, действующими в низких концентрациях. Лица с профессиональной гиперсекрецией являются группой риска в плане развития тяжелой патологии лёгких - хронического обструктивного бронхита.
Бронхоспазм - также нормальная реакция на действие ирритантов, обеспечивающая защиту паренхимы легких от воздействия. Ряд веществ вызывают бронхоспазм в концентрациях значительно меньших, чем вызывающие альтерацию легочной ткани (ФОС, карбаматы, диоксид серы). Другие (озон, аммиак) вызывают бронхоспазм в альтерирующих концентрациях, третьи (фосген) поражают паренхиму легких практически не провоцируя бронхоспазм.
Умеренный отек ткани воздухоносных путей - следствие повреждения эпителия ингалируемыми веществами. Однако этот эффект вызывается и стимуляцией аксонального рефлекса, через афферентные нервы дыхательных путей, причем порой при действии ксенобиотиков в очень незначительных концентрациях. При этом нервные окончания высвобождают низкомолекулярные биологически активные пептиды, так называемые тахикинины. Эти вещества вызывают вазодилятацию и усиление проницаемости сосудов (в воздухоносных путях - подслизистого слоя). Как показано в эксперименте, такие вещества как формальдегид, изоцианаты действуют таким образом.
В ряде случаев похожее состояние может развиваться в результате аллергического процесса. Микроскопия мазка выделений из носа может помочь провести дифференциальный диагноз между реакцией раздражения и аллергической реакцией. Большое число нейтрофилов в отделяемом из носа указывает на воспалительный характер поражения. Увеличенное содержание эозинофилов в мазке говорит об аллергической природе патологического процесса.
Повреждение слизистой дыхательных путей развивается при ингаляции токсикантов в достаточно высоких концентрациях. Повреждение эпителиальных клеток и их гибель запускают целый ряд процессов, пагубным образом сказывающихся на респираторном статусе пострадавших. Существенно снижается мукоцилиарный клиаренс; обычно тесный контакт между эпителиальными клетками нарушается, эпителиальный слой становится пористым (что позволяет бактериям проникнуть в ткани), а слущивание и отслойка мертвого эпителия может вызвать обструкцию дыхательных путей. Наконец активация синтеза и высвобождение поврежденными клетками различных цитокинов и медиаторов приводит к воспалительной реакции, отеку, спазму гладкой мускулатуры бронхов. Таким образом, прямое повреждение эпителия ингалируемыми токсикантами в высоких концентрациях существенно усиливает реакции, провоцируемые этими токсикантами в малых концентрациях.
Плохо растворимые в воде вещества пенитрируют при ингаляции в ацинусы, где вызывают повреждение альвеолярного эпителия, эндотелия альвеолярных капилляров, альвеолярных макрофагов. Особенно чувствительны к действию токсикантов пневматоциты 1 типа (причина - малая толщина и большая площадь поверхности клеток). Повреждение паренхимы легких приводит к развитию диффузной бронхиолярной обструкции вследствие отека, инфильтрации стенки бронхиол воспалительными клетками, а также выходу жидкости в просвет альвеол (отек легких). Повреждение макрофагов приводит к суперинфецированию и развитию химической пневмонии.
Значительно менее изучены механизмы формирования отсроченных во времени процессов, развивающихся вследствие острого воздействия.
Состояние большинства людей, перенёсших острое ингаляционное поражение, при адекватной терапии, нормализуется в течение нескольких суток - недель (в зависимости от степени тяжести), благодаря полной регенерации поврежденной ткани. Однако у некоторых лиц может развиться состояние повышенной чувствительности к токсикантам, проявляющаяся синдромом реактивной дисфункции дыхательных путей (СРДП). Вероятность развития СРДП выше у курильщиков. Веществами вызывающими СРДП и даже бронхиальную астму при однократной экспозиции являются изоцианаты (рисунок 4).
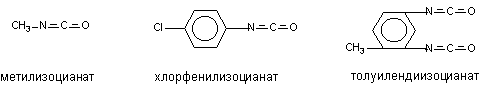
Рисунок 4. Структура некоторых изоцианатов
Отсроченное развитие ряда патологических процессов в легких может быть следствием не столько непосредственной альтерации легочной ткани токсикантом, сколько повреждения ее накапливающимися в паренхиме легких и дыхательных путях полиморфноядерными лейкоцитами. У части пораженных, перенесших острое воздействие химическим веществом, развивается прогрессирующий воспалительный процесс и, как следствие, облитерация глубоких отделов дыхательных путей (облтерирующий бронхиолит), что приводит к инвалидизации.
3.1.1. Локализация поражения
Как уже указывалось ранее, место действия токсиканта в дыхательной системе определяется его концентрацией, размером частиц (для аэрозолей), растворимостью в воде. Нередко вид токсиканта, вызвавшего поражение точно известен, как это бывает при разрушении цистерны с опасным веществом. Однако чаще ингаляционные поражение связаны с действием смеси веществ, находящихся как в форме газа, так и аэрозоля. Это имеет место при пожарах, авариях на объектах, на которых складируется, используется и производится множество веществ. Часто поражение утяжеляется присутствием в токсической смеси веществ, обладающих выраженным резорбтивным действием. Важным фактором, определяющим характер поражения дыхательных путей, является тип клеток, преобладающих в области преимущественного воздействия токсиканта. Клетки существенно различаются по их чувствительности к ксенобиотикам. Например, к диоксиду серы чувствительны не только эпителиальные клетки верхних дыхательных путей, но и гладкомышечные клетки этой области.
3.1.1.1. Верхние дыхательные пути
Патологические состояния, связанные с острым действием токсикантов на верхние дыхательные пути приводят к двум видам последствий: а) возбуждению рефлексов в силу раздражения нервных окончаний обонятельного, тройничного, языкоглоточного нервов (рефлекс Kratschmar), а также блуждающего нерва (рефлекс Salem-Aviado), сопровождающихся развитием апное, брадикардией, бронхоспазмом, кашлем, падением, а затем подъёмом АД (см. выше); б) развитием воспалительно-некротических изменений в дыхательных путях, выраженность которых определяется свойствами токсикантов и их концентрацией во вдыхаемом воздухе. Следствием воспалительно-некротических изменений является изъязвление слизистой, геморрагии, отек гортани. Хотя признаки поражения появляются довольно быстро отечная реакция развивается постепенно, а стридор (непроходимость гортани) может развиться через несколько часов после воздействия. У отравленных, наряду с поражением дыхательной системы, могут наблюдаться ожог кожи лица, глаз, ротовой полости, что затрудняет оказание помощи. Обычно, чем сильнее выражено поражение верхних дыхательных путей, тем выше вероятность поражения и глубоких. Перечень токсикантов, вызывающих раздражение и воспаление в дыхательных путях, представлен в таблице 4.
Таблица 4. Перечень наиболее известных токсикантов, вызывающих раздражение и воспалительные процессы в дыхательных путях
Ацетон Акролеин Акрилонитрил Алкилбензолы Аммиак Арсин и органические Бром Бутиловый спирт Диметил сульфат Диоксид серы Гексаметилен диизоцианат Иприты (сернистый, азотистый) Карбонил никеля Минеральные и органические кислоты (в форме паров и аэрозолей) |
Метилизоцианат Производные мышьяка Пентахлорфенол Пятихлористый фосфор Сероводород Толуол Тринитротолуол Треххлористый фосфор Хлористый метил Хлорнитробензол Хлористый цинк Хром Формальдегид Фосфин |
3.1.1.2. Глубокие дыхательные пути
Проявления поражения - от слабо выраженных явлений легкого воспаления (гиперемия слизистой, лёгкий отек и т.д.), до выраженных некротических изменений слизистой воздухоносных путей (псевдомембранозный процесс при поражении ипритом) и даже ожога легких (хлор в высоких концентрациях). Токсиканты, адсорбированные на поверхности ингалируемого аэрозоля, вызывают более тяжелые повреждения, чем действующие в газообразной форме. Так, при обследовании, в дыхательных путях жертв пожаров, подвергшихся воздействию токсикантов, выявлено наличие сажи и адсорбировавшихся на поверхности её частиц токсикантов.
Большинство случаев трахеобронхитов химической этиологии разрешаются практически без последствий (в случае поражения раздражающими ОВ в течение нескольких минут по выходе из зоны заражения). Однако выраженная экссудация, сопровождаемая спазмом дыхательных путей (облитерирующий бронхиолит), рефлекторным угнетением дыхательного и сосудодвигательного центров, - могут привести к асфиктическому синдрому (цианоз, диспное, потеря сознания).
Необходимо учитывать, что проявления острого трахеобронхита могут развиваться как немедленно после действия токсикантов (вещества с выраженным раздражающим действием), так и отсроченно. Прогрессирующий отек дыхательных путей развивается постепенно, достигая максимума через 8 - 24 часа после воздействия. Через 48 - 72 часа, при тяжелых поражениях, наблюдается отслойка слизистой оболочки. Развивается, так называемый, псевдомембранозный трахеобронхит. Продолжительность скрытого периода зависит от свойств токсикантов. Тяжелое поражение токсикантом дыхательных путей может закончиться бронхоэктатической болезнью, стенозом трахеи.
Мероприятия по оказанию помощи включают использование средств защиты органов дыхания, немедленный (по возможности) вынос пострадавших из зоны заражения (транспортировка лёжа), назначение кислорода (но не под давлением), в случае отсутствия выраженной асфиксии - адреналин внутримышечно в дозе 0,5 - 1 мг (0,5 - 1 мл 0,1% раствора) для снятия отека и бронхоспазма, назначение глюкокортикоидов (кортизон, преднизолон), бронхолитиков, антибиотиков, средств, успокаивающих кашель.
3.1.1.3. Паренхима легких
3.1.1.3.1. Пневмонии
В группу острых пневмоний химической этиологии входят различные, чаще комбинированные поражения, морфологические особенности которых определяются особенностями токсического действия ксенобиотиков. Пневмонии возникают, как при ингаляционном поражении, так и при иных путях поступления в организм токсикантов, выводящихся преимущественно через легкие (бензины). Токсические вещества, вызывающие химические пневмонии представлены в таблице 5.
Таблица 5. Вещества, вызывающие острую химическую пневмонию
Акролеин Аммиак Бензин Бериллий Диоксид серы Кадмий Хлористый цинк Формальдегид |
Керосин Марганец Соляровое масло Пятиокись ванадия Пары минеральных кислот Пары ртути Иприты Мышьякорганические соединения |
Токсиканты повреждают паренхиму лёгких, захватывая как альвеолярную стенку (острый, иногда геморрагический экссудативный альвеолит), так и легочный интерстиций (диффузная интерстициальная пневмония) (аспирация бензина, керосина, кадмий, марганец). В тяжелых случаях происходит некротизация легочной ткани и суперинфицирование с формированием абсцессов (акролеин), обструктивного поражения дыхательных путей (диоксид серы), клеточных интерстициальных инфильтратов (бериллий, кадмий). Нередко острое воздействие приводит к развитию длительно и вяло текущих токсических процессов. Ингаляция пыли, содержащей двуокись и закись марганца, может вызвать тяжелую пневмонию без суперинфицирования. В основе процесса лежит выраженный альвеолит, сопровождающийся формированием моноцитарного инфильтрата.
Лечение пневмоний химической этиологии осуществляется по общим правилам лечения этого недуга. К числу специфических средств терапии следует отнести введение комплексообразователей при интоксикациях металлами, антиоксидантов, при поражении веществами, в основе действия которых лежит активация свободно-радикальных процессов.
3.1.1.3.2. Отек легких
Характерной формой поражения легких токсикантами является отек легких. Суть патологического состояния - выход плазмы крови в стенку альвеол, а затем в просвет альвеолы и дыхательных путей. Отечная жидкость заполняет легкие - развивается состояние, обозначавшееся ранее как "утопление на суше".
Выделяют три типа отёка лёгких:
- гемодинамический отек лёгких, в основе которого лежит повышение давления крови (выше 30 мм Hg) в малом круге кровообращения, при отсутствии повреждения альвеолярно-капиллярной мембраны;
- собственно токсический отек лёгких, развивающийся в результате первичного поражения альвеолярно-капиллярной мембраны, на фоне нормального в начальном периоде внутрилегочного давления крови (давление в левом предсердии ниже 12 мм Hg);
- отек легких смешанного типа, когда у пострадавших отмечается как нарушение свойств альвеолярно-капиллярного барьера, так и сократительных свойств миокарда и т.д.
Основные токсиканты, вызывающие формирование отека легких представлены в таблице 6.
Таблица 6. Некоторые токсиканты, вызывающие отек легких
1. Вещества, вызывающие гемодинамический отёк лёгких: этиленгликоль цианиды оксид углерода арсин фосфин таллий кадмий фосфор ФОС и др. |
2. Вещества, вызывающий собственно токсический отек легких: аммиак оксид кадмия хлор хлорпикрин тетрахлординитроэтан метилсульфат кислород (при длительной ингаляции под повышенным давлением, озон) фосгег дифосген диоксид серы оксиды азоты пятифтористая сера паракват трехфтористый хлор и др. |
3. Вещества, вызывающие отек смешанного типа: дихлорэтан трихлорэтилен люизит и др. |
Собственно токсический отек легких связан с поражением токсикантами клеток, участвующих в формировании альвеолярно-капиллярной мембраны. При этом показано, что особенностью процесса является, прежде всего, усиление проницаемости легочных капилляров на фоне мало измененного гидростатического давления в малом круге кровообращения. Развивающееся состояние рассматривают как форму респираторного дистресс-синдрома взрослых (РДСВ).
Опыты на лабораторных животных показывают, что сразу после воздействия токсикантов снижается содержание сурфактанта в легочной ткани. Этим объясняется раннее развитие периферических ателектазов у пораженных. Потеря сурфактанта может иметь значение и для усиления проницаемости легочных мембран. Некоторые представления о патогенезе развития токсического отека легких суммированы на рисунке 5.
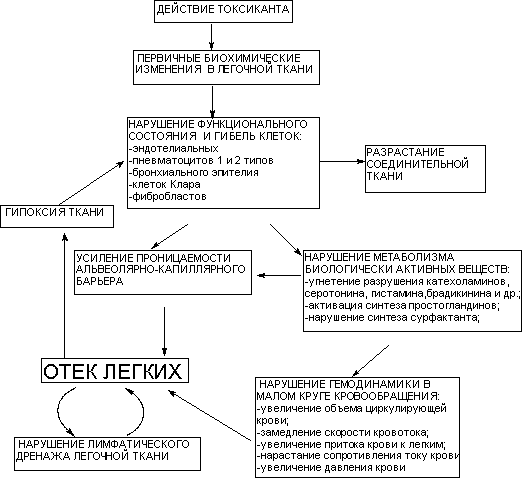
Рисунок 5. Схема патогенеза токсического отека легких
Помимо указанных на схеме изменений, для развития отека легких большое значение имеют системные нарушения, включающиеся в процесс и усиливающиеся по мере его развития: нарушения газового состава крови (гипоксия, гипер-, а затем гипокарбия), изменение её клеточного состава и реологических свойств (вязкости, свертывающей способности), расстройства гемодинамики в большом круге кровообращения, нарушение функции почек и центральной нервной системы. Смерть наступает от острой сердечной недостаточности.
Степень поражения легких токсикантами отражается на общем состоянии пострадавшего (таблица 7).
Таблица 7. Основные признаки острого поражения легких озоном различной степени тяжести
Показатели состояния |
Степени поражения |
|||
легкое |
умеренное |
Сильное |
тяжелое |
|
Изменение показателей при спирометрии |
5 - 10% |
10 - 20% |
20 - 40% |
> 40% |
рО2 в крови (ммHg) |
Более 50 |
около 50 |
около 40 |
менее 40 |
Продолжительность процесса |
Восстановление в течение 30 минут |
Восстановление в течение 6 часов |
Восстановление в течение 24 часов |
Восстановление в течение более 24 часов |
Признаки поражения |
Легкий кашель |
Кашель; боль за грудиной при глубоком вдохе; учащенное, поверхностное дыхание |
Кашель; сильная боль за грудиной при глубоком вдохе; учащенное, поверхностное дыхание; тошнота; головокружение |
Сильный кашель; боль за грудиной при дыхании; нарушение ритма дыхания; нарушение ориентации; потря сознания (рО2 - менее 30 ммHg) |
Ограничение активности |
Отсутствует |
Определяется у отдельных лиц |
Определяется у значительной части лиц |
Определяется у всех пострадавших |
(M. Lippmann, 1988)
Осложнениями отека легких являются бактериальная пневмония, формирование легочного инфильтрата, тромбоэмболия магистральных сосудов.
Смертность при этом грозном патологическом состоянии составляет, как правило, 5 -10 %, причем в первые 3 суток погибает около 80 % от общего количества погибших.
Острое отравление паракватом сопровождается в ряде случаев, вслед за отеком (или без него), развитием внутриальвеолярного диффузного фиброза. Лёгочный фиброз формируется в течение нескольких недель после приёма per os токсических доз вещества. На начальном этапе отмечается инфильтрация альвеол профибробластами, которые, созревая, закупоривают альвеолярные мешочки. При этом разрушаются стенки альвеол, образуются коллагеновые волокна. Возможен смертельный исход вследствие быстро развивающейся гипоксической гипоксии. Частым осложнением перенесенного заболевания является эмфизема легких.
3.1.2. Острая дыхательная недостаточность
Дыхательной недостаточностью называется состояние, при котором внешнее дыхание не обеспечивает оптимальный газообмен в покое и при нагрузке. При этом парциальное давление кислорода в крови падает ниже 60 мм Hg (в норме 98), а парциальное давление углекислого газа повышается более 50 мм Hg (в норме 40). В ряде случаев (гипервентиляция, токсический отек лёгких), дыхательная недостаточность может протекать на фоне нормального или даже пониженного содержания СО2. Острая дыхательная недостаточность может стать следствием любого описанного выше патологического процесса, обусловленного действием токсикантов.
В целом, основными причинами дыхательной недостаточности легочного типа при отравлениях являются:
- альвеолярная гиповентиляция вследствие угнетения дыхательного центра, слабости или паралича дыхательной мускулатуры, острого обструктивного синдома (спазм бронхов, гиперсекреция, отек воздухоносных путей);
- нарушение свойств альвеолярно-капиллярной мембраны (отёк легких, фиброз);
- нарушения соотношения объёма вентиляции и гемоперфузии легких.
Во всех случаях развивается близкая по сути последовательность событий, которую можно представить следующим образом: гипоксемия с гиперкарбией (или без неё) ® тканевая гипоксия ® активация анаэробного дыхания ® усиление продукции органических кислот (пировиноградной, молочной) ® метаболический ацидоз ® увеличение объема капиллярного русла и накопление крови в органах и тканях ® застойная гипоксия ® сокращение обратного венозного тока крови ® падение АД ® острое нарушение гемодинамики ® гибель.
Альвеолярная гиповентиляция (развивается при отравлениях ингибиторами АХЭ: ФОС, карбаматами; в терминальных стадиях острых смертельных интоксикаций большинством токсикантов) характеризуется понижением количества воздуха, участвующего в газообмене в единицу времени (уменьшение дыхательного объёма - ниже 350 см3). В силу ослабления вентиляции ацинусов устанавливается равновесие газов в средах: альвеолярный воздух - кровь, на новом, патологическом уровне. Кровь транспортирует кислород к тканям под давлением ниже 98 мм Hg. Подключающиеся защитные механизмы (учащение, углубление дыхания) оказываются несостоятельными в силу ослабления хеморецепторного рефлекса.
Понижение диффузионной способности легких, не смотря на нормальный или увеличенный градиент парциального давления газов в крови и альвеолярном воздухе. У нормального человека диффузионная способность О2 составляет 15 - 20 см3 О2/mmHg/мин. При физических нагрузках эта величина в норме может возрастать в 4 раза. Основные причины снижения диффузионных свойств легких при интоксикациях: утолщение альвеолярно-капиллярной мембраны, уменьшение дыхательной поверхности лёгких (токсический отек легких, токсические пневмонии). Итогом этих нарушений является инициация патофизиологических реакций, представленных выше.
Изменение соотношения вентиляция - перфузия (все интоксикации, сопровождающиеся коллапсом). У здорового человека соотношение объёмов ингалируемого воздуха и перфузируемой через легочную ткань крови варьирует от ацинуса к ацинусу, от одного отдела лёгочной ткани к другому, но в целом составляет 0,8 (4 литра воздуха и 5 литров крови в минуту). Как гемоперфузия не вентилируемых альвеол, так и вентиляция недостаточно кровоснабжаемых участков легких, приводят к понижению степени оксигенации оттекающей от легких крови. Формирующаяся гипоксимия провоцирует запуск цепи событий, описанных выше.
Типичными проявлениями острой дыхательной недостаточности являются снижение парциального давления кислорода в крови (рО2 ниже 20 mmHg несовместимо с жизнью), одышка, в тяжелых случаях падение АД, ацидоз, цианоз, нарушение сознания вплоть до комы.
3.1.3. Диагностика
Первым шагом на пути выявления лиц, подвергшихся острому воздействию токсикантов, является констатация самого факта воздействия. В тех случаях, когда этот факт очевиден (в лицо рабочему выброшена струя токсического агента), процедура носит формальный характер (регистрация случая). Однако значительно чаще это не простая задача.
Поскольку транзиторные токсические реакции быстро исчезают, а стойкие признаки острого ингаляционного поражения формируются постепенно, диагностика развивающейся патологии в ранние сроки представляет известную сложность. Рентгенографические изменения в легких в первые часы после воздействия отсутствуют; содержание газов в крови - в пределах нормы. Существуют косвенные признаки, позволяющие предположить возможность поражения пульмонотоксикантами. К их числу относятся: ожег кожи лица, слюнотечение, затруднение дыхания и т.д. Лиц, доставленных из зоны пожара (особенно при возгорании синтетических материалов) или взрыва в закрытом помещении всегда следует рассматривать как потенциально отравленных. Особое внимание следует уделять пострадавшим, находящимся в бессознательном состоянии, поскольку вероятность получить тяжелое отравление у них выше (см. выше).
Определенную помощь в диагностике может оказать обычная спирометрия или исследование объема форсированного выдоха в минуту (снижение показателей в силу раннего бронхоспазма).
Во всех случаях интоксикаций при пожарах следует определять содержание карбоксигемоглобина в крови. Как правило, уровень карбоксигемоглобинемии хорошо коррелирует со степенью поражения не только СО, но и другими токсикантами.
За пораженными устанавливается тщательное наблюдение. Периодически проводятся клинико-диагностические исследования (частота дыхания, ЭКГ, анализ крови, рентгенография легких, газовый состав крови и т.д.). Значительный ацидоз косвенно указывает на высокую вероятность поражения токсикантами, угнетающими тканевое дыхание (цианиды, сульфиды и др.). Прецизионной методикой ранней диагностики надвигающегося токсического отека легких является исследование диффузионных свойств легких. Показания к принятию решений по оказанию помощи пораженным представлены в таблице 8.
Таблица 8. Показания к принятию решений по оказанию помощи пораженным
Показания к госпитализации: - поражение в замкнутом пространстве - возгорание синтетических материалов - нарушение сознания - ожог кожи лица - загрудинные боли - респираторные синдромы (кашель, одышка) - карбоксигемоглобинемия |
Показания к оказанию неотложной помощи: - угнетение сознания - гипоксия - снижение объёма форсированного выдоха |
Показания к интубации: - ларингоспазм - тяжелый отек гортани - острая дыхательная недостаточность, угрожающая жизни |
3.1.4. Оказание помощи
Все лица, доставляемые из очагов ингаляционного поражения различными токсикантами подлежат госпитализации сроком не менее, чем на сутки. Оказание неотложной помощи, помимо мероприятий, направленных на устранение причины формирования угрожающего жизни состояния, включают: восстановление проходимости воздухоносных путей, искусственную вентиляцию лёгких, оксигенотерапию (иногда оксигенобаротерапию), профилактику осложнений.
Система оказания помощи при развивающемся токсическом отеке легких включает следующие мероприятия:
1. Снижение потребления кислорода (покой, тепло, назначение успокаивающих и противокашлевых средств);
2. Борьба с гипоксией (вынужденное положение тела, ингаляция противовспенивающих средств, кислородотерапия);
3. Профилактика отека (ингаляция и системное введение стероидных противовоспалительных препаратов, S-содержащих препаратов: унитиола, пенициламина; аскорбиновой кислоты);
4. Снижение объема крови, циркулирующей в малом круге кровообращения (вынужденное положение тела; нитроглицерин; форсированный диурез; жгуты на конечности; кровопускание);
5. Стимуляция сердечной деятельности (сердечные гликозиды);
6. Борьба с осложнениями (антикоагулянты; антибиотики);
Общая продолжительность лечения пострадавших - около 15 - 20 дней, осложненных форм - 45 - 55 дней.
Поскольку при экстремальных ситуациях пострадавшие часто имеют сопутствующие поражения (ожоги, шок) и нередко нуждаются в переливании большого количества жидкостей, оказание им помощи весьма затруднено. Необходимо отметить, что ожег кожи без поражения дыхательной системы, также сопровождается усилением проницаемости альвеолярно-капиллярной мембраны и, иногда, развитием отека легких.
3.1.5. Краткая характеристика некоторых пульмонотоксикантов
3.1.5.1. Хлор
Хлор - газ желтовато-зеленого цвета с характерным удушливым запахом, примерно в 2,5 раза тяжелее воздуха, хорошо растворяющийся в воде. Является сильным окислителем. Он сохраняется и транспортируется в сжиженном виде под повышенным давлением. В случае аварий возможно массовое поражение людей.
Уже в минимальных концентрациях (10 мл/м3) хлор раздражает дыхательные пути, действуя в более высоких концентрациях, вызывает тяжелое поражение. По данным А.А. Лихачева (1931) при регистрации гибели экспериментальных животных (собак) в течение трех суток LCT50 составляет около 70 г мин/м3 (при 15 - 30 минутной экспозиции).
Хлор был первым веществом, примененным на войне в качестве ОВ. 22 апреля 1915 г близ Ипра германские части выпустили его из баллонов (около 70 т), направив поток газа, движимый ветром, на позиции французских войск. Позже вещество широко применялось на фронтах 1-й Мировой войны и потому клиника поражения хорошо изучена.
В редких случаях смерть может наступить уже при первых вдохах зараженного воздуха. Причина смерти - рефлекторная остановка дыхания и сердечной деятельности. Другой причиной быстрой гибели пострадавших (в течение 20 - 30 минут после вдыхания вещества) является ожег легких. В этих случаях окраска кожных покровов пострадавшего имеет зеленоватый оттенок. При вскрытии обнаруживаются сухие на ощупь, спавшиеся легкие, зеленовато-серого цвета. Левое сердце пусто, правое расширено и наполнено густой кровью.
Чаще в случаях тяжелого отравления в момент воздействия пострадавший ощущает резкое жжение в области глаз и верхних дыхательных путей, стеснение дыхания. Отравленный стремится облегчить дыхание, разрывая ворот одежды. Одновременно отмечается крайняя слабость, вследствие этого отравленные падают и лишаются возможности бежать из пораженной зоны. Практически с начала воздействия появляется надрывный, мучительный кашель, позже присоединяется одышка, причем в дыхании участвуют добавочные дыхательные мышцы. Пораженный старается занять положение, облегчающее дыхание. Речь невозможна. Иногда наблюдается рвота.
Через некоторое время после выхода из зоны поражения может наступить некоторое облегчение состояния (скрытый период), однако чаще (в отличие от поражения фосгеном) полная ремиссия не наступает: сохраняется кашель, болезненные ощущения по ходу трахеи и в области диафрагмы.
Через некоторое время (от нескольких часов до суток) состояние вновь ухудшается, усиливаются кашель и одышка (до 40 дыхательных актов в минуту), лицо приобретает синюшную, а в крайне тяжелых случаях пепельную, окраску. Над легкими прослушиваются хрипы. Пострадавший постоянно отхаркивает пенистую желтоватую или красноватую жидкость (более 1 л за сутки). Наблюдаются сильнейшие головные боли, температура тела понижается. Пульс замедлен. Артериальное давление падает. Пострадавший теряет сознание и погибает при явлениях острой дыхательной недостаточности. Если отек легких не приводит к гибели, то через несколько часов (до 48) состояние начинает улучшаться, отечная жидкость рассасывается. Однако заболевание постепенно переходит в следующий период - осложнений, во время которого обычно развиваются явления бронхопневмонии.
Как правило, отравленные, не погибшие в первые 24 часа после воздействия, выживают. Явления бронхита и пневмонии могут наблюдаться в течение нескольких недель, а легочная эмфизема оказывается стойким последствием интоксикации. Часто в качестве осложнения регистрируются длительные нарушения со стороны деятельности сердца.
В подавляющем большинстве случаев поражений легкой и средней степени тяжести через известное время наблюдается полное восстановление здоровья.
3.1.5.2. Паракват
Паракват является контактным неселективным гербицидам. В 1955 году его стали широко использовать в сельском хозяйстве. Основными поставщиками пестицида являются Китай, Тайвань, Италия, Япония, Великобритания и США. Применение ядохимиката разрешено более чем в 130 странах.
Паракват - кристаллическое вещество белого цвета, без запаха. Хорошо растворяется в воде и спиртах; температура кипения 300о С (при этом препарат разлагается). Применяется паракват в виде крупнодисперсного аэрозоля (300-600 мкм). После выседания аэрозольных частиц на почву агент быстро разрушается с образованием малотоксичных продуктов. Поэтому даже при интенсивном использовании ядохимиката не отмечено его накопления в окружающей среде.
При воздействии коммерческих растворов вещества возможны местные обратимые повреждения кожи, ногтей, слизистых глаз. Общая интоксикация развивается только при приеме через рот. Токсичность параквата для млекопитающих достаточно высока (таблица 9). Смертельная доза для человека составляет приблизительно 3-5 г/чел.
Таблица 9. Токсичность параквата для грызунов (ЛД50 , мг/кг)
Путь введения |
Крысы |
Мыши |
||
самцы |
самки |
самцы |
Самки |
|
внутрь |
223 |
256 |
360 |
290 |
подкожно |
27 |
32 |
41 |
37 |
внутрибрюшинно |
25 |
27 |
4 |
- |
Основной причиной случаев отравления людей являются суицидные попытки. После приема вещество всасывается из тонкого кишечника и распределяется в организме. В желудочно-кишечном тракте всасывается не более 20% яда. Легкие активно аккумулируют паракват через механизм захвата биогенных аминов.
Действуя в дозах выше среднелетальных, вещество поражает все жизненно важные органы (печень, почки, легкие). Развиваются: ожог слизистой желудочно-кишечного тракта, диаррея, повреждение паренхиматозных органов и острый токсический альвеолит. Характерна отсроченная гибель отравленных через несколько дней или недель от нарастающего фиброза легких.
Поражение легких при интоксикации паракватом протекает в две фазы. В первую - деструктивную (1 - 3 сутки) - наблюдается гибель и десквамация альвеолоцитов 1-го и 2-го типов, что становится причиной острого альвеолита, токсического отека легких. Во второй фазе - пролиферативной - происходит замещение альвеолоцитов кубовидными клетками, постепенное разрастание фиброзной ткани.
В механизме токсического действия параквата ведущую роль играет образование в результате его метаболизма активного промежуточного продукта, инициирующего в клетках свободнорадикальный процесс. Повреждение мембран вследствие активации перекисного окисления липидов, сопровождается гибелью клеток, формирующих альвеолярно-капиллярный барьер. Наиболее чувствительны к параквату альвеолоциты I типа. Возможно, что в основе повреждения клеток лежит не только активация ПОЛ, но и другие механизмы.
Важную роль в процессе разрастания соединительной ткани в легких играют альвеолярные макрофаги и нейтрофилы крови. Эти клетки, активированные паракватом, продуцируют специфические гликопротеины, усиливающие пролиферацию фибробластов и их фиксацию на базальной мембране альвеол.
Предотвратить накопление параквата в легких после его приема на практике не удается. Субстраты-конкуренты яда (цистамин, путресцин и т.д.) могут оказать эффект лишь в ранние сроки от начала интоксикации (первые 8-12 часов). Лечение отравлений, помимо средств симптоматической и патогенетической терапии, включает назначение антиоксидантов: аскорбиновой кислоты (500 мг/кг), восстановленного глутатиона (14,4 мг/кг), витамина Е (30 мг/кг), витамин А (3000 ЕД на мышь)и т.д.
При отравлениях паракватом абсолютно противопоказана оксигенотерапия. Данное мероприятие достоверно ускоряет гибель отравленных. Только в случаях угрожающей жизни гипоксемии (РО2 в артериальной крови менее 40 мм Hg) возможна ингаляция кислорода.
Для профилактики фиброза легочной ткани применяют глюкокортикоиды.
3.1.5.3. Цинк
Цинк представляет собой голубовато-белый металл, находящийся в группе II периодической таблицы элементов. При нагревании выше 5000 цинк окисляется и испаряется в форме мельчайших частиц оксида цинка, которые в холодном воздухе подвергаются флокуляции с образованием дыма.
С древнейших времен человек использовал сплав цинка с медью и оловом (бронза), но вероятно не был знаком с чистым металлом вплоть до 15 века.
Мировая продукция металла в настоящее время составляет более 7 млн. тонн в год. Цинк и его соединения широко используется в хозяйственной деятельности.
Цинк является эссенциальным элементом организма. Высокое содержание его отмечается в предстательной железе, мышцах, поджелудочной железе, костях, почках.
Токсичность металла и его соединений мала. Наибольшую опасность представляют ингаляционные поражения дымами, содержащими соединения цинка, и аэрозолем оксида цинка. Так, после вдыхания ZnO в концентрации около 600 мг/м3 в течение 45 минут у кошек сразу после извлечения из камеры отмечаются нарушение координации движений, тремор, затруднение дыхания, понижение температуры тела.
Вследствие своих раздражающих свойств, хлорид цинка вызывает воспалительное повреждение кожи и поражения глаз. Ингаляция пыли, содержащей соли цинка, сопровождается раздражением слизистой оболочки верхних дыхательных путей.
Ингаляция паров и дыма, содержащего металлический цинк в высоких концентрациях приводит к формированию респираторного дистресс-синдрома, который может развиться спустя несколько суток после ингаляции, а в малых концентрациях - состояния, называемого "лихорадка литейщиков". Проявления синдрома включает: металлический вкус во рту, сухой кашель, учащение дыхания, утомляемость, миалгии, лихорадку, озноб, развивающиеся спустя 4 - 12 часов после воздействия. Температура может подниматься до 400. Количество лейкоцитов достигает 20000. Продолжительность приступа 1 - 3 часа. Со стороны ЦНС наблюдаются неспецифические эффекты типа ощущения усталости, вялости. Полная нормализация состояния - в течение 24-48 часов. Осложнения не наблюдаются. Достаточно быстро (в течение суток от начала контакта) формируется толерантность к действию металла, однако столь же быстро (1-2 дня) она исчезает. В этой связи характерно приступообразное течение этого вида профессиональной патологии. Наблюдаемая картина проявляется особенно ярко в начале трудовой недели, после перерыва в действии вещества в выходные дни. Отсюда еще один термин, обозначающий процесс - "утренняя лихорадка понедельника".
При ингаляционном поражении соединениями цинка необходимы мероприятия, направленные на профилактику токсического отека легких. При развившемся респираторном дистресс-синдроме взрослых - оказание помощи по общим правилам.
3.2. Хронические патологические процессы химической этиологии
Наиболее частыми формами токсического процесса, развивающегося при длительном профессиональном или экологическом действии пульмонотоксикантов, являются вяло текущие воспалительные процессы, гиперреактивные состояния дыхательных путей, диффузный интерстициальный фиброз легких, гранулематоз, облитерация дыхательных путей, канцерогенез. Перечень токсикантов - наиболее частых причин указанных состояний представлен в таблице 10.
Таблица 10. Перечень токсикантов, вызывающих патологические состояния дыхательной системы при длительном воздействии
Диффузный интерстициальный фиброз: алюминий, асбест, бериллий, угольная пыль, кобальт, медь, коалин, пары ртути, никель, масляная аэрозоль (липидная пневмония), паракват, кремниевая пыль, тальк, некоторые лекарства (блеомицин, бисульфан, циклофосфамид и др.) |
Облитерирующий бронхиолит: аммиак, оксид кадмия, хлор, хлорпикрин, сероводород, метилсульфат, кислород по давлением, озон, фосген, диоксид серы, трихлорэтилен |
Гигантоклеточные пневмонии: кобальт, тяжелые металлы |
Канцерогенез: асбест, акрилонитрил, арсенаты и арсениты (триоксид мышьяка), бериллий, хлорсодержащие эфиры (хлорметиловый эфир), кадмий, хром, хроматы, бензпирен, иприты, никилевая пыль, табачный дым, винилхлорид |
3.2.1. Аллергические и гиперреактивные заболевания легких
В норме иммунная система обеспечивает защиту легких от неблагоприятных воздействий, в том числе и токсикантов. Однако при воздействии некоторых ксенобиотиков ответ порой оказывается искаженным. Причиной этого могут стать вещества:
- вызывающие неспецифические вялотекущие воспалительные процессы в лёгких;
- обладающие антигенными свойствами, в том числе, способные образовывать комплексные антигены, инициирующие специфический иммунный ответ (см. раздел "Иммунотоксичность").
Итогом таких воздействий являются:
а) профессиональная астма;
б) синдром реактивной дисфункции дыхательных путей;
в) экзогенный аллергический альвеолит;
г) пневмокониоз;
д) фиброз, гранулематоз легких, вызываемый металлами, способными оказывать сенсибилизирующее действие.
От 2 до 15% случаев бронхиальной астмы в индустриально развитых странах - следствие профессионально обусловленных воздействий токсикантов. Большинство промышленных агентов, вызывающих астму, обладает аллергизирующей активностью, хотя в условиях профессиональной деятельности или неблагоприятной экологической обстановки на организм действует, помимо "основного" токсиканта, совокупность факторов (курение, длительный прием лекарственных средств, неблагоприятные климатические условия и т.д.). Высокомолекулярные вещества, содержащиеся, например, в растительной пыли, биопрепаратах (белки, пептиды, ферменты: пепсин, щелочная фосфотаза, пероксидаза, рибонуклеаза и т.д.), выделениях животных, могут вызвать аллергизацию, провоцируя образование иммуноглобулинов (IgE, IgG). Низкомолекулярные вещества, такие как ангидриды кислот (в частности фталиевый ангидрид), альдегиды (в частности - формальдегид, глютаровый альдегид), кислоты, изоцианаты, акриламид-мономер, алифатические амины, пары металлов - могут действовать в форме связанных с белками гаптенов, также вызывая гуморальный и клеточный иммунный ответ. Формированию профессиональной астмы, как правило предшествует длительный контакт с токсикантом.
Вместе с тем встречаются случаи, когда уже однократное воздействие раздражающих газов, паров, дымов, включая хлор и аммиак, в высокой концентрации приводит к гиперчувствительности дыхательных путей (синдром реактивной дисфункции дыхательных путей - СРДП). СРДП характеризуется стойким повышением чувствительности дыхательной системы к ксенобиотикам, которое формируется спустя несколько часов после воздействия, сохраняется в течение нескольких недель и проявляется бронхоспазмом при контакте с веществом. Полагают, что в основе СРДП лежит прямое разрушение токсикантами тучных клеток с высвобождением в ткани легких, содержащегося в клетках гистамина и других биологически активных веществ. У части отравленных гиперчувствительность к токсикантам сохраняется на всю жизнь. В этой связи, даже после успешного излечения пострадавшего от острого ингаляционного воздействия ксенобиотика, необходимо установить за ним медицинское наблюдение, с тем, чтобы предотвратить возможность тяжелых осложнений.
Экзогенный аллергический альвеолит представляет собой процесс, развивающийся после воздействия органической пыли, паров ангидридов кислот, изоцианатов (особенно толуолдиизоцианата), бериллия. Нередко патология возникает у сельскохозяйственных рабочих, работников птицефабрик. Клинически, заболевание напоминает остро или хронически протекающую интерстициальную пневмонию. Острая форма сопровождается лихорадкой, ознобом, кашлем, затруднением дыхания, одышкой. Процесс, как правило, разрешается в течение 24 часов. Хронический процесс может быть следствием длительного действия многих токсикантов. Он проявляется кашлем, утомляемостью, потерей веса, учащенным дыханием, признаками фиброза легких.
По современным представлениям пневмокониоз шахтеров, силикоз и асбестоз - процессы, также сопровождающиеся иммунологическими сдвигами. В результате поступления в лёгкие угольной пыли, асбеста, кремния эти вещества фагоцитируются макрофагами, что является пусковым механизмом для выделения этими клетками лизосомальных энзимов. Разрушение лёгочной ткани протеазами, выделяемыми макрофагами, приводит к постепенному её замещению соединительной тканью, то есть фиброзу легких. У лиц с хроническим силикозом при этом отмечается повышенное содержание в крови иммунных комплексов, включая ревматоидный фактор и антитела к ядрам клеток, усиленный синтез IgA. У больных асбестозом обнаруживается угнетение активности клеток-киллеров и антителозависимых цитотоксических клеток, уменьшение числа Т-лимфоцитов, повышенное содержание иммунных комплексов и иммуноглобулинов в крови.
Наконец, аллергический компонент прослеживается при профессиональной патологии лёгких у рабочих металлоплавильных цехов. Около 15 металлов обладают свойствами аллергенов. В наибольшей степени этот феномен прослеживается в клинике хронического бериллиоза, гранулематоза лёгких, вызванного алюминием, титаном, хромом, никилем.
4. Оценка пульмонотоксичности ксенобиотиков в эксперименте
Оценка пульмонотоксичности ксенобиотиков осуществляется в опытах на лабораторных животных. При этом необходимо четко определить условия воздействия изучаемых веществ (концентрация, продолжительность экспозиции и т.д.) и критерии оценки выраженности развивающегося поражения.
В настоящее время опыты, как правило, выполняют на белых крысах, кроликах, беспородных собаках (преимущественно самцах), хотя для этой цели подходит любой вид млекопитающих. Животные перед экспериментом должны содержаться в условиях вивария на обычном рационе питания.
Условия аппликации веществ следует выбирать исходя из их свойств, целей и задач исследования. В любом случае они должны быть стандартизованы.
Действие жидких веществ изучают либо в паровой фазе (летучие агенты), либо в форме аэрозолей с различной степенью дисперсности. Генерацию аэрозолей осуществляют при помощи ультразвуковых генераторов, гидравлических или пневматических распылителей. Аэрозоли твердых веществ получают путем распыления порошков или растворов веществ, а также методом термической возгонки.
Конструкция стендовой установки (камеры) для исследований должна предусматривать возможность экспонирования различных видов лабораторных животных в статическом или динамическом режимах воздействия газа, пара, аэрозоли.
Статический режим экспонирования предполагает одномоментное введение в рабочий канал установки определенного количество исследуемого вещества, после чего производится перемешивание токсиканта в воздушной смеси при помощи вентилятора и определение его исходной концентрации (С0 - мг/м3) в камере. Оптимальное время экспонирования животного в этом режиме составляет 5-20 минут. За 1-2 мин до окончания экспозиции определяют конечную концентрации токсиканта в камере (Сt).
Фактическую токсодозу вещества, воздействовавшего на экспериментальное животное, рассчитывают по формуле:
Ct = (СО + Сt) t /2 , где
Ct - фактическая токсодоза, мг мин/м3;
t - время воздействия, мин.
При изучении пульмонотоксичности вещества в динамическом режиме воздействия к камере подключают источник (генератор) постоянной подачи газа, пара или аэрозоля. Продувку зараженного воздуха через камеру обычно проводят со скоростью:
- для газов - 25 л/мин.;
- для паров - 50-75 л/мин;
- для аэрозолей 150-250 л/мин.
После перемешивания вещества в камере определяют его концентрацию (С - мг/м3). Время экспозиции выбирают исходя из особенностей свойств токсиканта и целей исследования.
Фактическую токсодозу вещества, воздействовавшего на экспериментальное животное, рассчитывают по формуле:
Ct = C t , где
Ct - фактическая токсодоза, мг мин/м3;
C - концентрация вещества в камере, мг/м3;
t - время воздействия, мин.
В случае острого эксперимента, за животными, подвергшимися воздействию, в течение 2-4 суток ведут тщательное наблюдение.
Критериями оценки поражающего действия пульмонотоксикантов могут являться:
1. Количество погибших животных и распределение случаев гибели в течение определенного времени после воздействия;
2. Морфологические показатели поражения (макро- и микроскопические), регистрируемые у погибших и выведенных из эксперимента животных в различные сроки после отравления;
3. Органометрические характеристики легких, определяемые у погибших и выведенных из эксперимента животных;
4. Показатели функционального состояния органов дыхания и других органов и систем лабораторных животных;
5. Биохимические показатели.
На основе данных эксперимента определяют принятые в практике показатели токсичности исследуемых веществ (пороговые, эффективные, непереносимые, смертельные токсодозы) либо характеризуют выраженность эффекта (летальность, сроки гибели, степень повреждения легочной ткани, нарушений со стороны других органов и систем и т.д.) при фиксированной токсодозе исследуемого токсиканта.
5. Выявления пульмонотоксического действия профессиональных и экотоксикантов
Установление причинно-следственных связей между патологией дыхательной системы, выявляемой у обследуемого, и действием профессиональных неблагоприятных факторов химической природы, порой очень сложная задача. Алгоритм её решения представлен в таблице 11.
Таблица 11. Выявление профессиональных и экологических причин лёгочной патологии химической этиологии
Профессиональный анамнез: - характеристика профессиональной деятельности - потенциальные возможности воздействия токсикантов, в условиях производства |
Бытовые условия: - расположение жилища, температура воздуха в помещениях, вентилируемость, строительные материалы - использование токсикантов в бытовых целях (гербициды, пестициды, средства бытовой химии и т.д.) - хобби - привычки (курение, склонность к приёму алкоголя, лекарств) - профессии членов семьи |
Биологический мониторинг: - общемедицинское обследование - анализ газового состава крови - иммунологические тесты - физиологические тесты - рентгенографические исследования - анализ лёгочной ткани на содержание минералов |
Обследование рабочего места: - изучение перечня токсикантов, оценка степени их опасности, потенциальной способности вызывать лёгочную патологию - обсуждение характера работы обследуемого с руководством промышленного объекта, медицинским персоналом объекта - оценка профилактических мероприятий, проводимых на объекте - анализ воздуха рабочей зоны, оценка загрязненности рабочего места |
5.1. Профессиональный анамнез
Если начало профессионального заболевания отсрочено, либо характер воздействия токсиканта трудно поддается анализу, врачу необходимо получить информацию о видах работы, выполнявшейся лицом, воздействиях, которым лицо подвергалось в период работы. Необходимые данные получаются путём анализа документации или опроса обследуемого.
Важно собрать сведения о возможном воздействии токсикантов, не связанных с профессиональной деятельностью: путем длительного приёма лекарств, вследствие вредных привычек (курение), хобби и т.д. Поражение может быть следствием заноса токсиканта в жилище одним из членов семьи (работниками асбестовых производств).
5.2. Биологический мониторинг
Биологический мониторинг предполагает клинико-лабораторное обследование с привлечением рентгенографических, физиологических, иммунологических, химико-аналитических, морфологических и других методов исследования.
Примеры профессиональной патологии лёгких химической этиологии, выявляемой физиологическими методами исследования, представлены в таблице 12.
Таблица 12. Патологические состояния, сопровождающиеся нарушением функциональных проб
1. Обструктивный тип нарушений А. Отсутствует реакция на бронхолитики - бронхоэктазы (аммиак) - хронический бронхит (раздражающие дыми, угольная и иная пыль и др.) - хронические обструктивные заболевания легких - эмфизема (курение, кадмий, диоксид азота и т.д.) - обструкция верхних дыхательных путей - стеноз трахеи (следствие химического ожога дыхательных путей, новообразования) Б. Сохранена реакция на бронхолитики - профессиональная астма (острое, хроническое действие токсикантов) - синдром реактивной дисфункции дыхательных путей (острое действие токсикантов в высоких дозах) |
2. Рестриктивный тип нарушений - гигантоклеточные пневмониты (кобальт) - интерстициальный фиброз (кислород, нитрофурантион, паракват и др.) - пневмокониоз (антракоз, силикоз, асбестоз) |
3. Обструктивно-рестриктивный тип - облитерирующий бронхиолит (оксиды азота, диоксид серы) - бериллиоз - асбестоз - силикоз - хронический аллергический альвеолит (белковая пыль) |
5.3. Обследование рабочего места
Важным этапом постановки диагноза является обследование врачом-специалистом рабочего места. В ходе обследования осуществляется осмотр производства, собираются сведения, недоступные в поликлинических условиях.
В большинстве случаев рабочие не знают всего перечня химических веществ, с которыми им приходится контактировать в процессе работы, и, следовательно, не могут в полной мере оценить сопутствующий этому риск. Перечень токсикантов, с указанием степени их опасности, является важнейшим элементом, позволяющим медицинскому работнику осуществлять контроль состояния здоровья работающих, устанавливать причинно-следственную связь между фактом воздействия и развивающейся патологией. В ряде стран существуют законы, обязывающие иметь на производствах такие перечни.
В случае необходимости выполняются замеры концентраций интересующих веществ в воздухе рабочей зоны, на рабочем месте. Собирается информация о состоянии здоровья других лиц, работающих на этом производстве.
Итогом обследования является не только уточнение диагноза, но и рекомендации по улучшению условий труда.
<< Содержание |



 Федеральное государственное бюджетное учреждение науки
Федеральное государственное бюджетное учреждение науки