|
Медико-биологический
информационный портал
|
|
для специалистов |
|
ТОМ 1, СТ. 2 (стр. 25-31) // Декабрь, 2000 г.
Обоснование использования биологически активных добавок янтавит и митомин на основе янтарной кислоты Е.И.Маевский, Е.В.Гришина, А.С.Розенфельд Институт теоретической и экспериментальной биофизики РАН, Пущино, Московская обл., Россия, 142290.
"Не добыванию золота, а защите здоровья
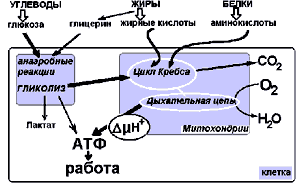
должна служить химия" Парацельс (1493-1541) Еще 2500 лет тому назад великий врач древней Греции Гиппократ показал, что, изменяя диету и уровень физической активности, можно лечить или, по крайней мере, облегчать течение многих болезней. Опыт народной и официальной медицины не только не противоречит представлениям Гиппократа, но существенно их расширяет и углубляет. Надеюсь, что любознательный читатель, обративший внимание на данную публикацию, великолепно информирован и о витаминах - необходимых компонентах пищи, не синтезируемых в организме человека, и о существовании множества видов лечебно-профилактических систем рационального питания, и о невероятном количестве пищевых добавок на нашем рынке. В этом сообщении мне хочется рассказать о Биологически Активных Добавках (БАД) к пище на основе Янтарной Кислоты (ЯК) - участнике внутриклеточного энергетического обмена. Для более глубокого понимания механизма влияния вводимой в организм ЯК, нам придется рассмотреть в схематичном виде некоторые стороны устройства энергетического обмена и место в нем ЯК. Принимаемые с пищей углеводы, жиры и белки расщепляются до простых соединений - глюкозы, глицерина, жирных кислот и аминкислот, которые в реакциях энергетического обмена, происходящих внутри клеток, превращаются в органические кислоты и затем окисляются до углекислого газа и воды (рис.1). Глюкоза и глицерин сначала окисляются анаэробно, то есть без участия кислорода, в ферментативных реакциях, называемых гликолизом. В тех ситуациях, когда доставка кислорода недостаточна, чтобы обеспечить функциональную нагрузку (работу) энергией, происходит активация анаэробного гликолиза, и в тканях накапливается конечный продукт гликолиза - молочная кислота (лактат). При достаточном кислородном обеспечении все органические кислоты сгорают в специализированных клеточных органеллах - митохондриях за счет потребляемого из воздуха кислорода (Рисунок 1)
Рис.1 Схема окисления углеводов, жиров и белков в реакциях энергетического обмена. Реакции гликолиза идут анаэробно (без кислорода) и завершаются накоплением лактата. В аэробных условиях продукты гликолиза, окисления жирных кислот и аминокислоты сгорают - окисляются с участием кислорода в митохондриях - клеточных органеллах, выполняющих роль основного источника энергии. Аккумуляция энергии в виде трансмембранного потенциала и АТФ происходит в дыхательной цепи - полиферментном комплексе, расположенном в мембране митохондрий.
Основная часть энергии солнца, заключенная в химических связях
потребляемых нами с пищей веществ, освобождается при окислении
органических кислот в циклической последовательности реакций,
открытых сэром Гансом Кребсом. Какие бы вещества ни служили
исходным топливом (белки, жиры, углеводы), в конечном счете все они
превращаются в органические кислоты Цикла Кребса. А далее идет еще
большая унификация топлива: при окислении органических кислот
отщепляется водород. И этот водород с помощью специального набора
ферментов - переносчиков дыхательной цепи переносится на
кислород. В итоге, именно в реакции взаимодействия водорода с кислородом
освобождается энергия. Но если в пробирке эта реакция идет с рассеиванием энергии в виде взрыва, то в организме лишь малая часть энергии освобождается в виде тепла, а большая часть аккумулируется в виде АТФ (аденозинтрифосфорной кислоты) и трансмембранных градиентов ионов. Цикл Кребса, дыхательная цепь и система аккумуляции энергии расположены в митохондриях. Митохондрии называют энергетическими станциями клетки. Именно в митохондриях все виды веществ сгорают до СО2 и Н2О, и митохондрии поставляют АТФ как универсальное энергетическое топливо для всех видов работ и синтезов. Количество и качество митохондрий, их функциональное состояние, взаимодействие с гликолизом и с системой доставки кислорода определяют диапазон функциональной активности клетки и соответствующей ткани. <В физиологических условиях: лимитирующим фактором обычно... служит количество доступного субстрата> Г.Кребс, Г.Корнберг, 1959. Превращение энергии в живых системах. В настоящее время мы знаем, что в основе многих эмпирически сложившихся систем питания лежит, прежде всего, воздействие на ключевые звенья энергетического обмена. Это легко понять, поскольку возможности энергетического обмена предопределяют объем и полноценность выполнения любой функции. Более того, оказывается, что эффективность любого регуляторного воздействия со стороны нервной и эндокринной системы также тесно связана с мобилизацией энергетического обмена. Любой управляющий сигнал - будь то гормон или нервный импульс на уровне организма или в системе внутриклеточной сигнализации - одновременно включает специфические исполнители и использование топливно -энергетических ресурсов. Ни один регулятор не работает в <голом> виде, без одномоментной и в большинстве случаев даже упреждающей подачи субстратов, необходимых для активации энергетического обмена исполнителя. Произвольная активация функций при умственной и мышечной работе является универсальным средством мобилизации и тренировки реакций энергетического обмена. И, наоборот, искусственная стимуляция - поддержание энергетического обмена позволяет осуществлять универсальную и мягкую регуляцию не только произвольных, но и не подчиняющихся, как правило, воле человека функций, например, вегетативной нервной системы. В связи с этим нельзя не отметить, что регуляция тонуса сосудов, частоты сердечных сокращений, функциональной активности печени, почек, секреция гормонов, моторная и секреторная функции желудочно-кишечного тракта, активность иммунной системы и множество других актов жизнедеятельности контролируются вегетативной нервной системой и другими регуляторными механизмами такого уровня, на котором воля человека, как правило, оказывается бессильной. Фармакологические препараты и различные методы нефармакологического лечебного воздействия на человека в значительной мере направлены на то, чтобы целенаправленно и специфическим образом управлять этими произвольно нерегулируемыми функциями. Этот путь развития медицинской науки чрезвычайно плодотворен, эффективен, но и опасен. Потому что очень трудно, если не невозможно, в такой сложной системе как человеческий организм изменять активность какой-то изолированной системы без нанесения ущерба другим системам.
Если же во главу воздействия на организм поставить влияние на
энергетически обмен - поддержание естественных обменных
процессов, необходимых для нормального и интенсивного функционирования
всех тканей, то у организма появляется возможность выбора в
соответствии с текущими рабочими потребностями разных клеток и тканей. А
контроль остается за самим организмом, его регуляторными
системами, отлаженными в процессе миллионнолетней эволюции.
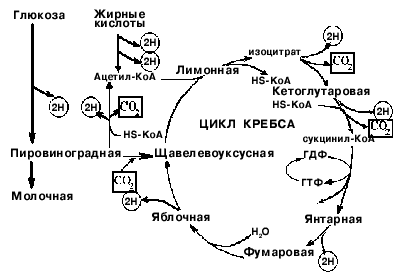
Рис. 2. Схема превращений субстратов в энергетическом обмене. Отщепление водорода (2Н) от субстратов - реакции окисления, в которых освобождающаяся энергия затем аккумулируется в виде АТФ.
Как показали исследования профессора Института теоретической и
экспериментальной биофизики Российской Академии наук Марии
Николаевны Кондрашовой, энергетическая мощность процесса синтеза
АТФ при окислении ЯК существенно выше, чем при окислении любого
другого субстрата. Именно поэтому многие энергозависимые, то есть
потребляющие энергию процессы, например, аккумуляция ионов
кальция и обеспечение биосинтезов водородом, даже в изолированных
митохондриях, могут идти лишь при окислении ЯК. Работами школы
М.Н.Кондрашовой показано, что в природе существуют и при
необходимости активируются дополнительные пути образования ЯК, а не
только те, которые приведены на рис. 2 в прямой последовательности
реакций Цикла Кребса. В частности, такое дополнительное
<впрыскивание> ЯК у здорового человека происходит при интенсивной работе и
в период восстановления после нагрузок, когда особенно высока
потребность в быстром воспроизводстве АТФ.
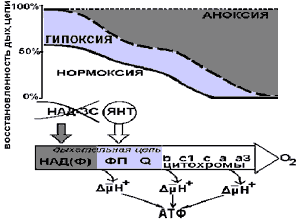
Рис. 3.Схема изменения степени восстановленности переносчиков дыхательной цепи митохондрий и пункты поступления водорода от НАД-зависимых субстратов и от ЯК в дыхательную цепь. Видно, что чем дальше от кислорода, тем выше степень восстановленности переносчиков даже в нормоксии. При гипоксии наиболее отдаленный участок дыхательной цепи целиком восстановлен и поэтому не может приянть водород НАД-зависимых субстратов Цикла Кребса. ЯК, в отличие от других субстратов, поставляет водород на участок, ближе стоящий к кислороду. Этот участок остается окисленным даже при гипоксии, что обеспечивает сохранение образования АТФ. Несмотря на то, что во время окисления НАД-зависимых субстратов образуется на одну молекулу АТФ больше, чем а при окислении ЯК, скорость окисления ЯК настолько выше, что в единицу времени больше АТФ образуется именно при окислении ЯК. В условиях гипоксии обычные кинетические преимущества ЯК относительно других субстратов возрастают из-за того, что дыхательная цепь открыта преимущественно для ЯК. Итак, при гипоксии окисление ЯК в митохондриях остается одним из немногих источников АТФ. Естественно было бы в такой ситуации дать источники ЯК или саму ЯК. Здесь нам хотелось бы обратить внимание читателя на то, что при кислородном голодании нельзя поддерживать только гликолиз (например, глюкозой), но необходимо сохранять митохондрии. Во-первых, чрезмерная активация гликолиза сопровождается развитием лактатного ацидоза (закислением тканей и крови вследствие накопления молочной кислоты), нарушением работы многих внутриклеточных ферментов, ионным дисбаллансом, нарушением механизма аэробного образования АТФ. Во-вторых, выживание во время и после кислородного голодания определяется сохранностью митохондрий. Вопрос о сохранности митохондрий пытаются решать путем пассивной защиты - "консервации" мембран, используя местные анестетики, ингибиторы фосфолипазы А2, антиоксиданты, комплексообразователи, связывающие ионы Са2+ и другие препараты, ограничивающие работу митохондрий. Из этого перечня в качестве компонентов БАД могут быть использованы прежде всего антиоксиданты ( природные в виде производных альфа-токоферола, бетта-каротина) или искусственные, в частности, синтезируемые в лаборатории Елены Борисовны Бурлаковой в Институте биохимической физики РАН. Однако живые системы невозможно эффективно сохранять путем ограничения их активности. В организме человека на всех уровнях те структуры, которые не функционируют, атрофируются и подвергаются деградации, в том числе и неработающие митохондрии. Нужны активные способы защиты, поддерживающие работу митохондрий, несмотря на дефицит кислорода. Такие способы выработаны в процессе эволюции. К ним относятся и механизмы гипоксического и анаэробного образования ЯК. Благодаря этим механизмам митохондрии способны выполнять роль источника энергии как при ишемии, так и при гипоксии. Использованию этого механизма при кислородном голодании для сохранения сердца посвящено множество работ, но мы особенно хотели бы отметить блестящие исследования в этом направлении доктора биологических наук Олега Ивановича Писаренко, руководителя лаборатории Кардиологического Научного Центра РАМН. В наших исследованиях, выполненных совместно с Еленой Владимировной Гришиной, удалось обнаружить наличие этих механизмов не только в митохондриях сердца, но и в головном мозге, печени и почках. Можно полагать, что эти механизмы представлены в митохондриях всех тканей. Отсюда ясно, почему поддержание системы образования и окисления ЯК в условиях кислородного голодания имеет ключевое значение для сохранения всех тканей. Особенно это становится актуальным при патологических состояниях, сопровождающихся развитием кислородного голодания. Внимательный читатель может упрекнуть меня в нелогичности. Если в организме существуют одновременно системы усиления образования и окисления ЯК, то незачем давать ее извне в пищевых добавках. Дело в том, что для запуска анаэробного образования ЯК необходимо наличие одновременно трех условий: высокой степени восстановленности дыхательной цепи, энергетического дефицита и, главное, достаточного количества источников для образования ЯК. Все эти условия создаются в результате глубокой гипоксии или ишемии. Заметим, что для успешного преодоления энергетического дефицита в организме существуют системы упреждающей мобилизации субстратов. Так выброс адреналина, включающего распад гликогена, повышающего уровень глюкозы в крови, улучшающего доставку кислорода к тканям за счет увеличения частоты и силы сердечных сокращений и частоты дыхания, происходит не тогда, когда в мышцах спортсмена снизится уровень богатых энергией соединений, а только от мысли о предстоящей нагрузке. Также поступаем и мы в том случае, когда даем БАД, содержащие ЯК или источники для гипоксического- анаэробного образования ЯК. Мы не ждем, когда разовьется гипоксический энергетический дефицит и будут сформированы условия для усиленного образования и окисления ЯК. Тем более, что далеко не у всех людей, тем более у больных или ослабленных, не тренированных по отношению к нагрузкам, имеется достаточно высокая активность соответствующих ферментов и эндогенные источники для достаточно эффективного образования ЯК и возможность успешно пережить гипоксический энергетический дефицит, включающий свои системы образования ЯК. Итак, мы подготавливаем ткани к гипоксической ситуации и облегчаем ее переживание за счет использования естественных метаболических путей и упреждения во времени развития энергетического дефицита. Такова идеология использования высоких субстратных доз ЯК.
Конечно, следует отметить, что при приеме даже нескольких
фасовок БАД, содержащих ЯК: таких, как Янтавит, Митомин или Энерлит,
человек получает относительно небольшое количество ЯК. Примерно в
100 раз меньше, чем давал своим пациентам Нобелевский лауреат
А.Сцент-Дьердьи в конце 30-х годов нашего столетия. И в 1000 раз
меньше, чем образуется ЯК в митохондриях в течение суток у любого
человека. Спрашивается, каким же образом такая малая доза внешней
ЯК может действовать на фоне огромных количеств собственной
эндогенной ЯК, образующейся в митохондриях в Цикле Кребса?
Ответ на этот вопрос очень прост. Так ЯК, которая образуется в
митохондриях моментально и сгорает в митохондриях, поэтому текущая
- стационарная концентрация присутствующей в тканях ЯК не
превышает в каждый момент времени 10-20 мг на кг массы ткани и, как
правило, из митохондрий не выходит. Вне митохондрий, вне клетки, в
кровотоке ее практически нет. Она появляется вне митохондрий при
тяжелом анаэробиозе (полном отсутствии кислорода) или при глубокой
гипоксии в каком-то участке ткани. Например, у ныряльщиков, или
при тяжелой интенсивной работе. Она может появляться вне
митохондрий и вне клетки при активации систем воспроизводства ЯК при
одновременном торможении ферментной системы окисления ЯК,
например, в условиях выраженного энергетического дефицита.
Если ресинтез АТФ происходит в реакциях гликолиза,
протекающего вне митохондрий, то утилизируются не все продукты распада
АТФ, а только АДФ и неорганический фосфат. Ионы водорода,
которые и являются кислотными эквивалентами, остаются в клетке и
выходят затем с избытком лактата в кровь. Если же энергообеспечение
осуществляют митохондрии, то утилизируются все продукты
гидролиза АТФ, включая ионы водорода. |
|||||||||||||
 Свидетельство о регистрации сетевого электронного научного издания N 077 от 29.11.2006 Свидетельство о регистрации сетевого электронного научного издания N 077 от 29.11.2006
Свидетельство о регистрации сетевого электронного научного издания Медлайн.Ру - N 227 от 20 октября 2008 года.
Выдано ФГУП "Информрегистр" Журнал основан 16 ноября 2000г.
Выдано Министерством РФ по делам печати, телерадиовещания и средств массовых коммуникаций
(c) Перепечатка материалов сайта Medline.Ru возможна только с письменного разрешения редакции
|
|
| Размещение рекламы | |
|
| |

 Articles
Articles