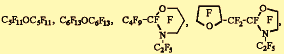|
Медико-биологический
информационный портал
|
|
для специалистов |
|
ТОМ 1, СТ. 1 (стр. 1-24) // Декабрь, 2000г.
БИОФИЗИКА НА ПОРОГЕ НОВОГО ТЫСЯЧЕЛЕТИЯ: ПЕРФТОРУГЛЕРОДНЫЕ СРЕДЫ И ГАЗОТРАНСПОРТНЫЕ КРОВЕЗАМЕНИТЕЛИ Г.Р. Иваницкий Институт теоретической и экспериментальной биофизики РАН Пущино Московской обл., 142290, Россия E-mail: ivanitsky@venus.iteb.serpukhov.su
Дается обзор работ, проведенных за последние 20 лет российскими
биофизиками совместно с химиками и клиницистами по созданию
перфторуглеродных газотранспортных эмульсий для биологических
и медицинских целей. Итогом этих исследований стал широко
применяемый в России коммерческий препарат - газотранспортный
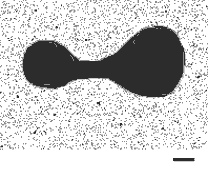
перфторуглеродный кровезаменитель перфторан. Ключевые слова: биомедицинская технология, перфторуглероды, газотранспорт. В последние годы медицинский мир разделился на два лагеря. Первый: переливание донорской крови приносит больше вреда, чем пользы. Второй: донорская кровь необходима, она - основное средство спасения жизни пострадавших. Продолжаются дискуссии. Ни один конгресс или симпозиум по трансфузиологии, хирургии или реаниматологии не обходится без обсуждения этой проблемы [1]. Донорская кровь - поцелуй смерти или дар жизни? "Чаша весов" склоняется в пользу первого утверждения. Главным аргументом в споре служит уже не только угроза переноса с донорской кровью многочисленных инфекций (СПИДа, вирусного гепатита, цитомегаловирусов, малярии, герпеса, вируса Эпштейна-Бара и многих других), но и реакции реципиентов на ее введение. Непрерывное открытие новых, ранее неизвестных инфекций, иммунологические проблемы совместимости (переливание крови - аналогично пересадке органов) и религиозные ограничения, запрещающие переливание человеку чужой крови, препятствует использованию донорской крови. Кроме того многочисленные техногенные катастрофы и локальные военные конфликты, когда возникает дефицит времени на определение групповой совместимости и необходимо сразу большое количество крови, требуют создания полноценных искусственных кровезаменителей [2-4]. Необходимость многочисленных тестов непрерывно удорожает донорскую кровь. Международная цена порции донорской крови для одной трансфузии уже колеблется в зависимости от группы крови от 150 до 200 $ США. Для пациента цена благодаря страховкам обычно удваивается, т.е. составляет около 300-400 $. Потребность в переливании крови огромна и составляет около одного переливания на 400?500 человек в год. Только для России необходима донорская кровь для 2-3 млн переливаний в год, что составляет около 1 млн литров. При этом следует заметить, что как показывает мировая статистика, при тщательном контроле донорской крови вероятность внесения инфекций реципиенту, хотя и небольшая, но существует всегда. Так, например, для ВИЧ-1, смешанных форм ВИЧ-1 и ВИЧ-2 и гепатита она составляет соответственно: 0,4.10-3, 0,5.10-3, 0,3.10-1 % на одно переливание. Кроме тестов на СПИД, сифилис, гепатиты А и В с 1994 года в России введена обязательная проверка на антитела к вирусу гепатита С, которым у нас по приблизительным оценкам заражены около 10 млн человек. В ряде стран развернулась кампания по пропаганде аутодонорства, т.е. создания индивидуального запаса своей крови для себя, чтобы в случае необходимости избежать переливания чужой [4]. Аутодонорство - это не панацея. Оно доступно лишь состоятельной части общества. Таким образом создание искусственных газотранспортных кровезаменителей, снимающих проблему групповой совместимости донорской крови, весьма актуально. Интерес к решению этой проблемы подогревается у фармацевтических компаний необъятностью рынка сбыта. По оценкам фирмы HemaGen (США), только в городах для применения в кардиопульмонологической хирургии и травматологии потребность мирового рынка составляет в ценах донорской крови от 1,9 до 2,9 млрд долларов в год. Модифицированный гемоглобин или перфторуглероды? Создание газотранспортных кровезаменителей на основе искусственного гемоглобина, несмотря на бурный старт [5-9], оказалось сложнее, чем ожидали. Межмолекулярные сшивки при создании полигемоглобина изменяют равновесные состояния между аминогруппами каждой отдельной молекулы гемоглобина и ограничивают подвижность ее альфа-и бетта-цепей. В результате гем либо плохо связывает, либо плохо отдает кислород, либо полигемоглобиновая молекула разваливается в кровеносном русле. При этом появляются многочисленные побочные эффекты [163-168, 172,173,176,182-189,191,197,198]. Несмотря на трудности, разработка модифицированного гемоглобина продолжается, и оптимизм не покидает исследователей [9,177,202,212]. Хотя значительного прорыва в доведении полигемоглобинового кровезаменителя до клинической практики в ближайшее время ожидать трудно. Альтернативой кровезаменителя на основе модифицированного гемоглобина являются перфторуглеродные эмульсии. Биофизиков заинтересовала не только их химическая устойчивость, но большая способность жидких перфторуглеродов растворять газы. Они растворяют до 50 объемных % кислорода и в 4 раза больше углекислого газа. Для иллюстрации приведу два эксперимента, которые в свое время привлекли к этому классу соединений внимание разработчиков кровезаменителей. В 1962г. Ж.Килстра (J.A.Kylstra) с соавторами опубликовал статью <Мышь как рыба> [10], в которой показал, что мышь может оставаться живой, будучи погруженной в физиологический раствор, который под повышенным давлением насыщается кислородом. Четыре года спустя Л.Кларк (L.Clark) и Ф.Голлан (F.Gollan) обнаружили, что такой эффект можно получить при нормальном атмосферном давлении, если вместо воды применить жидкий перфторуглерод [11]. Как бывает со всяким тонущим грызуном, его легкие наполняются жидкостью, но, к великому удивлению, он продолжает дышать. В опытах Кларка крыса дышала до 10 мин. Затем ее вынимали, удаляли жидкость, после чего она жила несколько дней. Кларк считал, что крысы погибали от воспаления легких. У нас этот эксперимент был повторен на мышах (рис.1).  Рис.1. Жидкостное дыхание.
Рис.1. Жидкостное дыхание.Мышь погружена в жидкий перфторуглерод, насыщаемый при атмосферном давлении и при комнатной температуре кислородом из воздуха. Поглощаемый из перфторуглерода кислород позволяет ей оставаться живой, находясь под слоем жидкости. В наших опытах они не выдерживали столь длительно пребывания под слоем жидкости. Перфторуглероды в 2 раза тяжелее воды и в 1000 раз тяжелее воздуха, поэтому мускулатура легких мыши не может долго выдерживать такую нагрузку. Однако принудительное прокачивание через легкие может позволить животному длительное время дышать такой жидкостью. И все же массированная подача чистых перфторуглеродов в легкие не проходит бесследно (многие чистые перфторуглероды модифицируют мембраны клеток альвеол). Чтобы избежать последствий от такого дыхания, необходимо использовать не один перфторуглерод, а готовить специальные эмульгированные смеси из двух или более разных перфторуглеродов. На этом аспекте проблемы ниже мы остановимся отдельно. Тем не менее столь наглядная демонстрация газотранспортных свойств перфторуглеродов сразу привела к идее использовать их как кровезаменители. В начале 80-х годов мы провели эксперимент со свободноплавающими инфузориями - тетрахименами (Tetrahymena pyriformis) [12].  Рис.2 Биоконвекция потребляющих кислород инфузорий тетрахимен в кювете толщиной 1,5
мм:
Рис.2 Биоконвекция потребляющих кислород инфузорий тетрахимен в кювете толщиной 1,5
мм:а) - фотография установившихся потоков движения (верхний рисунок) и схема движения тетрахимен (нижний рисунок) в от крытой кювете (кислород поступает в воду сверху из воздуха), б) - фотография потоков движения (верхний рисунок) и схема движения (нижний рисунок) тетрахимен в кювете, перевернутой и помещенной в чашку Петри с перфторуглеродом (кислород поступает в воду снизу через слой перфторуглерода). Эти инфузории обладают окситаксисом. Поскольку вода плохо растворят кислород (всего около двух объемных процентов), они периодически поднимаются к поверхностному слою за "глотком" кислорода, образуя при этом биоконвекционные потоки любопытной формы (рис.2а). Если кювету перевернуть и поместить в банку с жидким перфторуглеродом, рисунок траекторий меняется, так как теперь кислород поступает в воду из перфторуглерода (рис.2б). Инфузории не всплывают наверх, а двигаются по дну на границе раздела <вода-перфторуглерод>. Этот эксперимент, так же как и эксперимент с мышью-утопленницей, показал, что различные организмы - от инфузорий до млекопитающих - могут усваивать кислород, отдаваемый перфторуглеродами. Кто был первым? Вопросы приоритета в данном обзоре рассматривать не будем, т.к. трудно установить кому первому в мире пришла идея использовать фторуглеродные эмульсии как газотранспортные кровезаменители. Интенсивное их изучение для этих целей почти одновременно началось в конце 60-ых - начале 70-ых годов ХХ столетия в разных странах. Известны основополагающие работы, принадлежащие Л.Кларку (L.Clark), Р.П.Гейеру (R.P.Geyer), Ф.Голлану (F.Gollan), Р.Наито (R.Naito), К.Якояме (K.Yokoyama) [8,11,13,14] и другим. В целом в хронологии открытия и применения фторсоединений в биологии нет однозначности. Всегда трудно найти начало в процессе непрерывного развития науки. В конечном итоге важно не только кто первым стартовал, но и кто дошел до создания коммерческих препаратов. Первые соединения фтора начали использоваться отнюдь не в биологии, а в металлургии. Плавиковый шпат, другое его название флюор (от латин. fluo - теку, поскольку CaF2 делал расплавы и шлаки металлургических производств текучими), был описан еще в конце XY века. Отсюда и пошло в англоязычной литературе название фтора флюор. Сам химический элемент был открыт позднее в 1771 году К. Шееле, а в свободном виде был получен в 1886 году А. Муассаном.. Фтор сильнейший окислитель, активный неметалл, который реагирует со всеми элементами, кроме инертных газов, поэтому он взрывоопасен. В связи с этим этот элемент был назван в 1810 году французом А.Ампером фтором от греческого phthoros - разрушение. Русское название этого элемента заимствовано у Ампера, хотя во французском языке стали использовать его латинское наименование флюор. Химия фторных соединений интенсивно начала развиваться с 30-ых годов ХХ века и особенно в период и после 2-ой мировой войны в связи с потребностями атомной промышленности и ракетной техники. Потребности военных активно стимулировали развитие новых технологий. Газообразный фтор служил для разделения изотопов урана UF4 в UF6 , а также использовался как жидкий окислитель ракетного топлива. Развитие фторной промышленности заложило основы для поиска мирных применений фторных соединений, в том числе и в медицине [15, 16]. Тем не менее медико-биологические эффекты воздействия фтора и его соединений были известны давно. В молекулярном виде фтор в природе не встречается, но его соединения могут содержаться в подземных водах. С их особыми свойствами человечество столкнулось задолго до открытия самого фтора как химического элемента. Нормальное поступление фтора в организм человека 2,5-3,5 мг в сутки. Отступление от этого диапазона вызывает заболевания. Предельная допустимая концентрация для фтор-ионов в воде 0,7 мг/л. Как показали наши исследования, биологически безопасной является концентрация свободных ионов фтора в вводимых внутривенно перфторуглеродных препаратах не более 10-5-10-4 молей. Основной метод определения ионов фтора в жидкости - это потенциометрия с помощью селективных электродов. Подавляющее количество фтора в человеке и животных сосредоточено в их костях, до 100-300мг на кг. У человека из 2,6г фтора, содержащегося в организме, 2,5 г приходится на кости. Повышение содержания фтора опасно тем, что он связывает P, Ca, Mg и другие элементы, нарушая тем самым их баланс в организме, кроме того стимулируют активность некоторых ферментов. Первые медицинские применения фторсоединений были связаны с укреплением костей, прежде всего зубов. Эти соединения и сейчас широко используются в зубных пастах [16]. В нашей стране приступить к исследованиям в области перфторуглеродных кровезаменителей стало возможным в 70-ых годах, когда созданная под научным руководством академика И.Л.Кнунянца фторная промышленность начала искать медицинские приложения своей продукции. Военных прежде всего интересовал кровезамещающий препарат, который можно применять в условиях полевых госпиталей. Работы были засекречены, но не увенчались успехом, т.к. разработчики пошли по пути повторения японского препарата флюозол, воспроизведя его со всеми недостатками. Идея формирования открытой крупномасштабной междисциплинарной программы с привлечением специалистов разного профиля, в частности биофизиков, принадлежала Ф.Ф.Белоярцеву. Под его влиянием в 1979 году в Научном центре биологических исследований в г.Пущино было проведено первое организационное совещание, на котором была подготовлена программа совместных исследований почти 40 академических и отраслевых предприятий [17]. 10 апреля 1979 года проект программы "Перфторуглероды в биологии и медицине" был доложен на Президиуме Академии наук СССР, который констатировал важность этих исследований и поручил И.Л.Кнунянцу, Ф.Ф.Белоярцеву и мне (рис.3) подготовить предложения для Правительства СССР. 
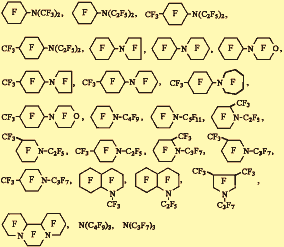
Рис.3 "На смотрины в Правительство" - шарж (август 1979 года) по мотивам картины В.Г.Перова "Тройка". Слева направо: Г.Р.Иваницкий, Ф.Ф.Белоярцев, И.Л.Кнунянц. Так появилась целевая комплексная программа под номером 42 (1980-1985) с девятью пунктами основных направлений: 1.Разработка метдов синтеза, получения и очистки новых перфторуглеродов, поверхностно-активных веществ, плазмоэкпандеров, изучение их физико-химических и биологических свойств. 2.Создание и медико-биологическая апробация оксигенаторов крови на жидких фторуглеродных мембранах. 3.Создание "искусственной крови", предназначенной для возмещения кровопотерь. 4.Создание газопереносящих перфузионных сред для региональной перфузии и сохранения изолированных органов в целях трансплантации. 5.Использование эмульсий перфторуглеродов для кардиоплегии и перфузии коронарных артерий в целях защиты миокарда от аноксии при операциях на "открытом" сердце. 6.Использование эмульсий фторуглеродов для терапии нарушений микроциркуляции и регионального кровообращения. 7.Культивирование клеток на фторуглеродных подложках и средах, модифицированных фторуглеродами. 8.Разработка методов легочного дыхания млекопитающих в жидких средах. 9.Использование эмульсий фторуглеродов в качестве инкубационных сред в лабораторных исследованиях с переживающими тканями. Главной целью этой программы было выполнение пункта 3. Первая англоязычная публикация, подытожившая его выполнение, появилась в 1983 г. "Ftorosan - oxygen carrying perfluorochemical plasma substitute" [18]. На нее и ссылались в англоязычной литературе [19], хотя ей предшествовали другие опубликованные на русском языке работы, выполненные в рамках этой программы [20-29]. Следует заметить, что названиями фторосан и перфторан именуется один и тот же газотранспортный перфторуглеродный кровезаменитель. Замена названия фторосан на перфторан была вызвана просьбой Фармакологического комитета Минздрава СССР. Название кровезаменителя, первоначально предложенное нами, было созвучно названию другого фторного препарата фторотан, который был физиологически активен. Фторотан (F3CCHClBr) - это средство для ингаляционного наркоза. Таким образом перфторан (фторосан) был создан еще в конце 1982 году, а разработка его началась в 1979 г. по инициативе автора этой статьи - биофизика и, главное, двух моих коллег - медика и химика. Ими был внесен наибольший вклад в постановку и решение этой проблемы, поэтому эти имена требуют особого упоминания - это профессор, доктор медицинских наук Феликс Федорович Белоярцев (1941-1985) и академик, генерал-майор инженер Иван Людвигович Кнунянц (1906-1990). К сожалению, они ушли из жизни, начав исследования, но не увидев их результат. С 1985 по 1990 годы начались события, которые иначе, как абсурдными не назовешь. Людям старшего поколения памятна история этого периода, когда началась травля разработчиков, а массовая печать была заполнена публикациями на эту тему. Успешно идущие клинические испытания перфторана были остановлены. Исследования по доведению отечественного перфторуглеродного кровезаменителя до клиники и массового производства были задержаны почти на шесть лет. К его качеству и эффективности это не имело никакого отношения. Эти события унесли из жизни наиболее активного их разработчика Ф.Ф.Белоярцева. Вряд ли целесообразно излагать эту историю, поскольку теперь она описана в книгах и в статьях [30,31], в том числе и в журнале Nature [32]. Только в 1990 году мне с сотрудниками удалось настоять на продолжении работ и возобновлении клинических испытаний. В результате перфторан прошел все стадии клинических испытаний (I и II фазы в 1984-1985гг. более 600 пациентов, III фаза в 1990-1995 гг более 200 пациентов), одобрен Фармкомитетом (22 декабря 1994г.), прошел регистрацию Фармакопейного комитета (30 августа 1995г.), получил регистрационное удостоверение (13 февраля 1996г.) и лицензию на массовое производство Министерства здравоохранения Российской Федерации (21 апреля 1997г.). Препарат зарегистрирован как новое поколение кровезаменителей, обладающих газотранспортной функцией, улучшаюших газообмен и метаболизм на уровне тканей, повышающий кислородный транспорт крови, обладающий мембраностабилизирующей функцией, восстанавливающий центральную гемодинамику, обладающий протекторным действием на миокард и блокирующим медленные входящие кальциевые токи. Также он обладает сорбционными, диуретическими свойствами, улучшает динамику кровотока и периферическую микроциркуляцию крови. Здесь нет смысла приводить его химический состав и физико-химические свойства, т.к. теперь все эти сведения легко найти во многих доступных публикациях [например 3,33- 35]. В 1999 году разработчики, внесшие наибольший вклад в создание перфторана, были удостоины премии Правительства Российской Федерации . Ф.Ф.Белоярцев получил эту премию посмертно. К сожалению, мы часто говорим о лидерах нашей науки в прошедшем времени, похоронив их. В процессе создания этого препарата ежегодно (за исключением вынужденного перерыва 1985-1990гг.) проводились научные конференции. Теперь их направленность в большей степени стала клинической. По результатам конференций выпускаются тематические сборники статей. В сборниках достаточно полно отражены результаты, полученные на различных этапах работы. Всего было выпущено 10 таких сборников [36-45]. Сейчас готовится к выпуску 11-ый. Однако многие из них стали библиографической редкостью и далеко не все библиотеки, даже в России, их имеют. Часть их содержания дублировалась в текущей научной периодике, которая более доступна. В списке литературы сделан акцент на эти публикации. Для удобства читателя ссылки содержат полное название работ. Ссылки на тезисы из-за их огромного количества в список литературы не включены. Кроме того по этой тематике защищено 9 докторских [46-54] и 29 диссертаций кандидатов наук [55-84]. Дальнейшее изложение пойдет по схеме: развернутые ответы на шесть вопросов, которые на разных этапах работы чаще всего задавались оппонентами. Такая форма избрана как наиболее удобная для изложения специфики воздействия перфторуглеродов на живые объекты. Частично фторированные или недофторированные соединения обладают физиологической активностью и многие из них весьма токсичны. Так, гексафторбензол - это ингаляционный анестетик (используемый в ветеринарии); уже упоминавшийся фторотан (F3CCHClBr) - средство для ингаляционного наркоза; фторбензол, дифторбензол, полициклические фторароматические соединения - полупродукты в синтезе пестицидов; 5- фторурацил - известный убийца РНК, используемый в химеотерапии рака [15,16]. Инерционность мышления с переносом свойств недофторированных соединений на полностью фторированные первоначально культивировала негативное отношение ко всем соединениям фтора и породила вопрос. Не возникнут ли у перфторуглеродных эмульсий токсические эффекты? Если соблюдены технические требования на содержание свободного иона фтора (<10-4 М) и осуществлено полное фторирование углеводородных соединений, то токсической активности не будет. По сравнению с органическими соединениями перфторуглероды являются химически весьма устойчивыми. Если в углеводородах все водороды заменить на фтор, то будут получены перфторуглеродные соединения или перфторуглероды (ПФУ). Приставка "перфтор-" указывает на полное замещение. Иногда приставку перфтор заменяют латинской буквой F, реже греческой буквой ф(фи) ( например, перфтордекалин или F-декалин или -декалин ) [16]. К классу перфторорганических соединений (ПФОС), которые могут найти применение в медицине, относятся не только перфторированные углеводороды, но и перфторированные третичные амины, перфторированные простые эфиры и полиэфиры. Последние отличаются от перфторированных углеводородов тем, что в своем составе содержат наряду с атомами углерода атомы азота или кислорода. Часто, хотя это не совсем верно, наименование ПФУ и ПФОС используют как синонимы. Мы в обзоре будем использовать для всех ПФОС сокращение ПФУ или F-углероды . Перфторуглероды разлагаются при температурах около 600-10000С. При обычных температурах не реагируют с концентрированными кислотами, сильными окислителями, металлами и щелочами. Эти реакции возможны лишь с температур 200-4000С. Разложение крупных молекул ПФУ на смеси их фрагментов или выделение свободного иона фтора может происходить в условиях радиолиза или жесткого ультразвука. Поэтому ПФУ- эмульсии медицинского назначения нельзя готовить с помощью ультразвуковых дезинтеграторов и стерилизовать радиационным облучением. С щелочными металлами ПФУ реагируют только при очень сильном нагреве (свыше 2000С) или в жидком NH3 при температуре 200С. Поскольку в организме такие условия отсутствуют, то ПФУ-соединения не метаболизируются. Необходимо пояснить причины их химической инертности, их две [85,86]. Во-первых, необычная прочность ковалентных связей C-F ( энергия химической связи 120 ккал/моль) [86]. Для сравнения энергия ковалентной связи С-Н составляет 99 ккал/моль. Во-вторых, особая стереохимия ПФУ-молекул. Длины связей F и H с углеродом соизмеримы 1,39A и 1,09A, но атом F в 19 раз тяжелее атома водорода. Молекулы перфторуглеродов такие же компактные как молекулы аналогичных углеводородов, но весьма плотные и тяжелые. Перфторированные соединения покрыты "шубой" из атомов фтора, все связи которых ковалентно замыкаются на атомы углерода, находящиеся внутри. Это дало основание химикам образно назвать их "веществами с алмазным сердцем и шкурой носорога" [85]. Твердые ПФУ-соединения (например, тефлон) более устойчивы к действию концентрированных кислот и щелочей, чем благородные металлы - золото и платина. Поэтому твердые F-углероды стали кандидатами для создания на их основе различных протезов для медицины: искусственных сосудов, клапанов сердца, специальных раневых покрытий ("искусственной кожи"), а жидкие - "искусственной крови". На рис.4 показаны примеры перфторорганических соединений, синтезированных в процессе выполнения работы сотрудниками академика И.Л.Клунянца [36].
На рис.5 показана химическая структура основных жидких F-углеродов, нашедших применение при создании кровезаменителей. 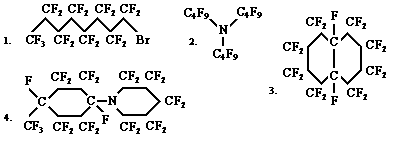
Рис.5. 1 - F-актилбромид (C8F17Br; 499; 4 дня; 50/210); 2 - F-трибутиламин (C12F27N; 671; 900 дней; 39/152); 3 - F-перфтордекалин (C10F18; 462; 7 дней; 40/190); 4 - F-метилциклогексил-пиперидин (C12F23N; 595; 90 дней; 40/150). В скобках указаны формулы, молекулярный вес в далтонах, период полувыведения из организма и соотношение растворения О,sub>2 к CO2 в объемных процентах. Приведенные перфторорганические соединения используются: 1-ый в американском кровезамещающем препарате - оксиджент; комбинация 2-3-его в японском кровезамещающем препарате - флюозол DA; комбинация 3-4-ого в российском кровезамещающем препарате -перфторан. Для отбора наиболее перспективных для медицины перфторуглеродов использовалась комплексная система тестирования, основанная на совмещении физико-химических, клеточно-органных и физиолого-анатомических методов контроля (табл. 1).
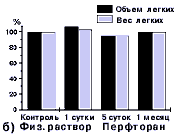
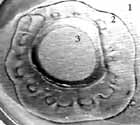
Однако химическая инертность ПФУ-соединений полностью не сняла вопрос о биологической активности эмульсий на перфторуглеродной основе, а породила другой вопрос. Не будут ли эти препараты при введении в организм давать побочные эффекты, вызывая не химические, а физические структурные перестройки в каких-либо органеллах, клетках или органах человека? Поводом для сомнения в безопасности использования эмульсии F-углеродов была оценка величины их поверхности. В 1,2 -1,5 литрах перфторана - 20% весовой эмульсии (допустимая доза для человека) содержится порядка в 1017-1018 перфторуглеродных частиц со средним размером 0,07 мкм. Такое их количество, сорбируясь на поверхности мембран, может покрыть двойным слоем площадь порядка 1000-2000м2. На первый взгляд эти цифры впечатляют. Однако, в сопоставлении с реальными поверхностями мембран живых организмов, на которых они могли бы сорбироваться, эти цифры ничтожно малы. У человека суммарная поверхность капилляров легких 120*103 м2, суммарная поверхность остальных капилляров порядка 15*103 м2, поверхность всех эритроцитов порядка 3,5*103 м2, а суммарная поверхность митохондрий фантастически большая 105 м2. Даже, если взять поверхность только капилляров легких и принять как гипотезу, что все частицы, сорбируются на этой поверхности, то они смогут покрыть только 1-2% этой поверхности. Если бы они все сорбировались на поверхности эритроцитов, то смогли бы покрыть не более 10% их поверхности. Но главное состоит в том, что такое сорбционное представление о взаимодействии F-углеродов с мембранами далеко от реальных процессов. Обычно в фармакологии дозировка лекарственных соединений рассчитывается на кг веса организма. Критерием опасных доз является показатель ЛД50 (летальная доза, когда 50 % численности в популяции экспериментальных животных, которым введен препарат, выживают). Например, ЛД50 перфторана при внутривенной инъекции мышам составляет 140 мл/кг. Для человека с большим запасом безопасности допустимая доза перфторана установлена в 20 мл/кг. При этой дозе как показали многочисленные эксперименты на различных животных и наблюдения в клинике перфторан не продуцирует гемолитических эффектов, не пирогенен, не вызывает анафилактоидных реакций, не ингибирует гемопоэз, не тератогенен и не эмбриотоксичен, не канцерогенен и не приводит к патологическим изменениям органов [ 36-38,89,90]. Что касается структурных перестроек органов, то, например, при взаимодействии F- углеродов с тканью легких (конечным пунктом их основной концентрации и выведения из организма) в экспериментах на крысах была выявлена следующая кинетика (рис.6): при дозах введения перфторана в пересчете на вес содержащихся в них перфторуглеродов 6г/кг замечено незначительное временное увеличение объема и веса легких на 2-3%, затем такое же уменьшение и приход в норму. Контролем для перфторана служил физиологический раствор. Электронно-микроскопические исследования показали, что это связано с образованием под действием макрофагов "перфторосом" - вакуолей, наполненных перфторуглеродами, которые затем раскрываются и перфторуглероды испаряются во внешнюю среду, не оставляя никаких морфологических изменений в легких. Такая же систуация со всеми органами [90]. Через гематоэнцефалическиий барьер F-углероды не проходят. При непосредственном воздействии на нейроткань в культуре клеток они аккумулируются в астроглии и в дальнейшем выводятся [91].
Рис.6. Влияние перфторуглеродов на органы: а) - электронно-микроскопическая фотография слоя F-углеродистой эмульсии перфторан, масштабная шкала 0,1мкм, средний размер частичек F-углерода 0,07мкм, частицы покрыты поверхностно-активным веществом проксанолом; б) - кинетика воздействия эмульсии на легкие крыс состоит из трех этапов: первоначальное незначительное разрыхление ткани легких (1-ые сутки), затем ее уплотнение (5 сутки) и, наконец, приход в норму (1месяц). Однако в силу своей сорбционной способности некоторые F-углероды могут легко образовывать комплексы с цитохромом (эксперименты были проведены на микросомальных мембранах печени крыс). Первоначально активация F-углеродами синтеза цитохрома в печени вызывала опасения. Уровень цитохрома на третьи сутки даже после введение перфторана в 2-3 раза превышал контрольное значение и составлял 1,8 н.моль/мг белка. Увеличение содержания микросомального цитохрома сопровождалось увеличением скорости окисления свободного НАДФН в 2-2,5 раза. Только на 10-ые сутки все приходило в норму. Это могло означать, что печень реагирует на введение перфторана как на мутаген или канцероген. Дальнейшие исследования показали, что это не так страшно, как казалось вначале. Перфторан индуцировал синтез цитохром П-450 аналогичной появляющемуся при фенобарбиталовом воздействии. Эта изоформа отличается от индуцируемой полициклическими углеводородами, например бензапиреном и другими канцерогенами (цитохром П-448). Более того активация синтеза цитохрома П-450 даже полезна, т.к. активирует монооксидазные реакции печени в отношении барбитуратов. Это явление можно использовать для детоксикации организма при отравлениях липофильными ксенобиотиками [53,160]. К мутагенезу и канцерогенезу она отношения не имеет. Кроме того комплесообразование F-углеродов с цитохромом П-450 коррелирует с их гидрофобно- липофильным индексом и размером частиц в эмульсии. Поэтому может быть снижено до допустимых норм соответствующим подбором F-углеродов и дисперсного состава эмульсии [92-97]. Следует заменить, что до сих пор среди некоторых разработчиков существует стремление использовать для кровезаменителей F-углероды, которые быстро выводятся из организма. Ошибочность этой стратегии аргументируется ответом на следующий вопрос. Не будет ли часть F-углеродов растворяться в липидах мембран, модифицируя их? Действительно, молекулы F-углеродов, (также как молекулы проксанола - поверхностно-активного вещества, используемого для получения эмульсий [99]), могут растворяться в липидах и тем самым модифицировать мембраны и даже воздействовать на их каналы и рецепторы [20,28,29]. Однако при правильном подборе смесей F-углеродов в одних случаях это явление можно практически исключить (при создании кровезаменителей), а в других - усилить (например, при получении эмульсий для консервации органов для трансплантации) [100-120]. С растворимостью F-углеродов в оливковом масле и в мембранах эритроцитов хорошо коррелирует такой их параметр как критическая температура растворимости в Н-гексане (КТРГ). Липофильные F-углероды с низким значением КТРГ ( как например, F-декалин, КТРГ=220С) быстро выводятся из организма. Период полувыведения - порядка 5?7 суток. Для липофобных F-углеродов с высоким значением КТРГ (например, F-трибутиламин, КТРГ=610С) скорость выведения небольшая, поэтому период полувыведения резко увеличивается и может достигать 900 суток. Оказалось, что КТРГ - параметр, чрезвычайно чувствительный к деталям структуры F-углеродов (наличие или отсутствие циклов, гетероатомов, вид разветвленности и т.д.). Он может быть рассчитан даже для еще не синтезированных молекул F-углеродов. Именно таким образом в рамках этих исследований в ИНЭОСе РАН И.Л.Кнунянцем с сотрудниками была в 1981 году "сконструирована" молекула перфтор-N-(4- метилциклогексил)пиперидина (ПМЦП), который является умеренно липофильным (КТРГ=380 С, период полувыведения 90 дней) [121]. По сути - это компромиссное решение, т.к. необходимо учитывать еще одну функциональную характеристику F-углеродов - способность образовывать устойчивые эмульсии. Ключевым параметром определяющим скорость разрушения эмульсии F-углерод/вода, является растворимость F-углерода в воде. Молекула ПМЦП с достаточно большим молекулярном весом характеризуется растворимостью в воде на 2 порядка меньшей по сравнению с F-декалином и вследствие этого устойчивость эмульсий ПМЦП приблизительно в 200 раз выше. Именно на основании этих данных была создана двухкомпонентная рецептура перфторана: 2 части F-декалина, обеспечивающего высокую скорость выведения, и 1 часть ПМЦП, повышающего устойчивость результирующей эмульсии и "гасящего" реактивный F-декалин, сильно модифицирующий мембраны клеток. Поэтому гидрофобно-липофильный индекс, то есть растворимость в воде и в Н-гексане, был использован в качестве одного из основных параметров для синтеза и скрининга F- углеродов медико-биологического применения. Он характеризует управление регуляторно- приспособительными механизмами клетки путем: модификации мембран, изменения реакции рецепторов клетки на эту модификацию, скорости выведения F-углеродов из организма и образования комплексов с цитохромом П-450. Этот индекс - температурозависимый. Было показано, что можно подобрать такие композиции эмульсий F- углеродов и поверхностно-активных веществ, при которых обеспечивается избирательное воздействие на ионную проводимость каналов мембран клетки, например, блокирование каналов Са2+ при отсутствие изменения каналов Na+ и К+ [28,29]. Блокирование каналов Са2+ при гипоксии в некоторых случаях может оказаться весьма полезным. Например, хорошо известно, что повышение уровня Са2+ в плазме кардиомиоцитов вызывает сокращение миофибрилл, а его удаление - их расслабление. В условиях массивной кровопотери, при операциях на остановленном сердце или при подготовке сердца к трансплантации избыток Са2+ может привести к контрактуре сердечной мышцы, т.е. к явлению, так называемого, "каменного сердца". Это такое состояние сердца, при котором его кардиомиоциты, а точнее их миофибриллы, находятся в состоянии глобального сокращения, что не только не позволяет сердцу выполнять насосную функцию, но и чревато тем, что после нормальной подачи кислорода сердце не сможет выйти из состояния сокращения. F-углероды, помимо подачи О2 , воздействуя на кальцевую проводимость мембран снижают концентрацию Са2+ в кардиомиоцитах, и тем самым уменьшают вероятность развития гиперсокращения миофибрилл. При блокировке Са2?-каналов сократительная функция сердца временно понижается, но поскольку макроэргические фоcфаты миоцитов снижаются медленно, то сердце не погибает, а продолжает работать в консервативном режиме, обеспечивающем сохранность его тканей. Следует подчеркнуть, что эксперименты на изолированным сердцем и с его фрагментами являются удобными моделями для подбора рецептур F-углеродных кровезаменителей, поскольку сердце - это быстро реагирующий орган на колебания подачи кислорода [110,111,114]. Хотя сердце составляет всего 0,5% от веса организма, но оно в покое потребляет 10% поступаещего О2, а при активной работе потребление кислорода возрастает в 3-4 раза. Эмульсии с соответствующим подбором F-углеродов позволяют не только защищать миокард при операциях [46,80,117], но и консервировать донорские органы (сердце, почки, легкое), предназначенные к трансплантации [58,101-103,106,116]. Не будут ли F-углероды при их испарениии с поверхности легких приводить к "вспениванию" мембран? Действительно такой процесс может наблюдаться при неправильно подобранных F- углеродах [94,97]. Недавно удалось создать простую и наглядную модель этого явления [123]. Был обнаружен феномен самопроизвольного движения липида в системе из трех несмешиваемых жидкостей: F-углерод - липид - вода, сопровождаемый возникновением потока пузырьков (липогазосом), направленных в липиде от F-углерода к воде. Разрываясь на периферии, пузырьки создавали газолипидные протуберанцы (рис.7). Рис.7. Схема расположения в чашке Петри трех несмешиваемых жидкостей: 1 - вода; 2 - липид; 3 - перфторуглерод. а) - Мгновенная фотография картины движения б) - Вид сверху на чашку Петри с сечением по линии АА 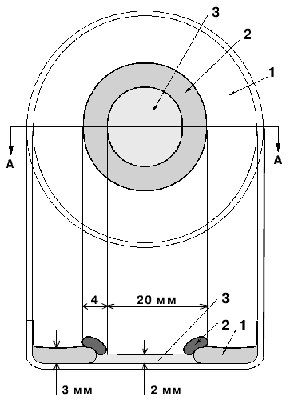
Подвижность липидного слоя возникает спонтанно за счет появления на границе "вода/перфторуглерод" температурного градиента, который зарождается благодаря отличию теплот испарения, упругости пара, поверхностного натяжения и газорастворяющей способности воды и перфторуглерода. Этот эксперимент наглядно подтверждает возможность вспенивания липидов и дает метод подбора F-углеродных смесей, исключающих такое явление на мембранах клеток.
Не будут ли F-углероды на долгий период оставаться в организме? Были проведены исследования на крысах, кроликах и других животных по определению времени удержания и локализации F-углеродов в их органах [21,36,37,42,84,89,90]. Концентрацию F-углеродов в тканях животных и в их крови определяют с помощью пламенного хроматографа или ЯМР-спектроскопии. Динамика выведения F-углеродов эмульсии перфторан из кровеносного русла кроликов при введении ее в дозе 20 мл/кг показана на рис. 8а, а на рис 8б приведена динамика выведения различных F-углеродов из органов крыс после 65-70 % замены крови [84]. Из графиков видно, что F- декалин выводится быстро (еще быстрее выводится F-октилбромид). Однако по этой причине их использовать вне смесей с медленно-выводящимися F-углеродами нельзя. Высокое давление их паров и низкое поверхностное натяжение приводят к <вспениванию> мембран легких и уже в дозе 2-4 г/кг к смертельному исходу для животных. Смеси двух F- углеродов, например, для перфторана - 2 части F-декалина и 1 часть F- метилциклогексилпиперидина (ПМЦП) даже в дозах 30 мл/кг (что соответствует 6г/кг), не наносят вреда животным. Но при этом один из F-углеродов, а именно ПМЦП, выводится из организма медленно. В табл.2 представлены замеры содержания ПМЦП в органах животного [84]. Эта таблица дает представление о фармакодинамике медленно выводящейся компонеты перфторана из органов крысы.
Первоначально столь значительное время удержания медленновыводящихся F- углеродов в организме грызунов смущали клиницистов, т.к. казалось, что время удержания F-углеродов в организме человека должно быть еще больше по сравнению с лабораторными животными, т.к. скорость процессов метаболизма у мелких животных выше, чем у человека. Дальнейшие исследования показали, что такие опасения напрасны. Общее время ? нахождения F-углеродов в организме складывается из суммы двух времен: t = tкр + tорг (1), где tкр - время нахождения эмульсии F-углеродов в кровотоке, tорг - время нахождения F-углеродов в тканях органов. Желательно, чтобы первое слагаемое tкр было большим, а второе маленьким. Чем дольше частицы эмульсии не покидают кровеносное русло, тем выше газотранспортная эффективность кровезаменителя. Величина первого слагаемого tкр действительно зависит от скорости метаболизма животного. Разрушение частиц F-углеродной эмульсии в кровотоке происходит как под действием механических (частота и перепады артериального давления), так физико- химических нагрузок (перепады кислородного напряжения и выброса О2, периодических изменений pH вдоль по руслу кровотока). Например, у мыши и крысы частоты пульса соответственно 498 и 350 ударов в минуту, что в 5-6 раз чаще, чем у человека. Удельная (приведенная к весу) величина потребления кислорода мышью и крысой соответственно составляют 2 мл/г час и 0,88 мл г час, а у человека всего 0,35 мл/г час и т.д. Поэтому ?кр у мышей и крыс приблизительно в 3-6 раз меньше по срвнению с tкр для человека. Разрушаемые F-углеродные частицы и у грызунов, и у человека утилизируются макрофагами. Однако к величине второго слагаемого tорг скорость процессов метаболизма животного имеет косвенное отношение. Выведение F-углеродов из организма животных - это многостадийный процесс. В кровотоке и в органах частицы перфторуглеродов в основном концентрируются альвеолярными макрофагами, а также макрофагами печени, селезенки, костного мозга [21,84]. Захват частиц F-углеродов приводит к образованию в тканях органов "перфторосом", которые затем перемещаются макрофагами в апикальную часть к поверхности ткани. Далее следует выброс перфторуглеродов путем экзоцитоза [89,90]. Конечным основным органом, через который удаляются из организма млекопитающих перфторуглероды, являются легкие. Этот факт не является неожиданным, т.к. среди поверхностей организма, контактирующих с внешней средой, наибольшую поверхность имеют именно они. Например, в обоих легких взрослого человека находится свыше 700 млн альвеол, общая дыхательная поверхность которых около 90 м2, т.е. примерно в 45-50 раз больше других поверхностей организма, контактирующих с внешней средой. Для сравнения поверхность кожи человека составляет всего 1,5-2 м2. На порядок меньше поверхности других контактируемых с внешней средой органов. К тому же необходимо учесть и принудительную вентиляцию легких за счет дыхания (16-18 раз в мин). Хорошо известно, что у человека роль кожи в газовом обмене со средой невелика. Например, через кожу выделяется не более 1,4 % CO2 [124]. Аналогично и выделение паров перфторуглеродов через кожу (не более 1-2 %). В сравнительной физиологии для различных видов животных в связи с газообменом и отведением теплопродукции величины внешних поверхностей определены довольно точно. Если бы поверхность отвода тепла на единицу веса у кита была бы такой же, как у мыши, то температура его тела приблизилась бы к точке кипения воды. Природа <позаботилась>, чтобы поверхность, соприкасающаяся с внешней средой (поверхность обмена газами и теплопродукцией), по мере увеличения веса росла бы быстрее, чем степень 2/3 от веса. Анатомические и физиологические исследования показали, что для сравнения объема газообмена и отведения тепла для различных животных можно записать следующую зависимость [124]: M=KWb или что тоже самое logM=b logW+logK (2), где М - газовый или тепловой обмен [в единицах для газообмена мл/ч, а для теплоотдачи в единицах ккал/ч], W - вес в граммах, b - коэффициент 0,73-0,75 (он больше, чем 2/3), K - величина, определяющая начало кривой <газовый обмен или теплопродукция - вес>. Эта величина зависит от ряда условий и ее определяют путем экстраполяции до пересечения с осью ординат. В табл. 3 приведены расчетные значения относительного увеличения скорости выведения (испарения) перфторуглеродов из организма крупных животных по сравнению с их выведением из мыши. Скорость выведения перфторуглеродов из мыши принята за единицу. Для человека величина tорг будет приблизительно в 8 раз меньше, чем для кролика или в 3 раза, чем для собаки.
Кроме того на рис.9 приведен сводный график зависимостей tкр = f(W) и tорг = f(W). Он дает представление об увеличении tкр и уменьшении tорг в зависимости от веса и вида млекопитающих. 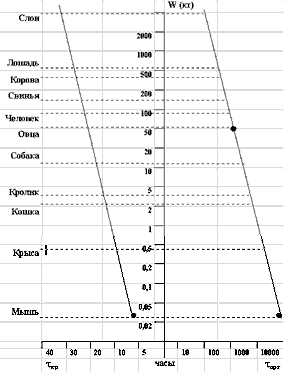
Рис.9. Ранжировка видов млекопитающих по времени нахождения перфторуглеродной эмульсии в кровотоке (справа) и по времени выведения перфторуглеродов из их органов (слева) в зависимости от среднего веса вида животного. В процессе выполнения работы экспериментальные данные были получены для мышей, крыс, кроликов и собак. Для других видов животных они вычислялись методом экстраполяции с учетом веса животного. Перфторуглероды растворяются в липидах, поэтому наряду с учетом поверхностей выведения необходим также учет вариаций фосфолипидов по видам органов животных. Тем не менее распространенное мнение, что перфторуглероды должны долгое время задерживаться в организме человека, опровергается клиническими наблюдениями. Времена выведения F-углеродов, которые определялись в эксперименте на мелких животных, переносить на человека можно лишь вводя поправки на различия в весе. Существенно ли влияние F-углеродов на процессы газотранспорта ? Это - главный вопрос. Приведем высказывание из дискуссий 80-ых годов: <О неэффективности использования эмульсий F-углеродов в качестве кровезаменителя - переносчика кислорода свидетельствуют, например, данные Tremper et al (1984 г), которыми показано, что при клиническом применении 20 % вес/об. эмульсии <Флюозола -ДА> (японский перфторуглеродный кровезаменитель - прим. автора) в дозе 20 мл/кг флюорокрит составляет приблизительно 3 %, что сооветствует 0,5г гемоглобина. Трудно представить, что дополнительные 0,5г гемоглобина смогли бы значительно повлиять на кислородный и гемодинамический статус больного> [125]. С другой стороны Lenard Clarк et al обнаружили, что при прямом определении напряжения кислорода в мозговой ткани у кроликов с помощью полярографических имплантированных электородов при инфузии перфторуглеродных эмульсий в условиях кровопотери, напряжение кислорода не соответствовало низкому суммарному уровню кислорода плазмы в кровяном русле [126]. Кроме того Дж. Остерхольм с сотрудниками из Медицинского колледжа им. Джефферсона (Филадельфия) в этот же период на животных с тяжелым ишемическим инсультом показал, что при введении эмульсии F-бутилтетрагидрофурана животные выживали даже в том случае, когда у них электроэнцефалограмма имела вид прямой линии (общепринятый критерий гибели мозга) [127]. Несложно доказать, что предмета для спора не существует, а есть недоразумение, а именно - путаница в понятиях <кислородная емкость> и <кислородный транспорт>. <Емкость> - понятие статическое, <транспорт> - динамическое. Можно иметь малую <емкость> сосуда и быстро его опорожнять, непрерывно доливая в него содержимое, обеспечивая тем самым большой <транспорт>. Рассмотрим нелинейные эффекты, которые имеют место в системе "перфторан + оставшаяся после потери кровь", и покажем, что эти эффекты вносят существенный дополнительный вклад в газотранспорт . Кислородная емкость 5-5,5 литров крови у человека при гематокрите 45 % и при давлении 100 мм.рт.ст. составляет порядка 20 об. %, т.е. около одного литра. Тот же объем физиологического раствора или плазмы имеет кислородную емкость всего 2-2,4 об.%, т.е. порядка 100 мл. Любопытно отметить, что кислородная емкость 1 литра крови в процентном отношении такая же как 1 литра воздуха, то есть благодаря гемоглобину весь организм становится <прозрачным> по кислороду и внутренние органы имеют потенциальную возможность (если она реализуется) получить такое же <довольствие>, как и наружные [129]. Еще одно физиологически важное свойство крови: при переходе артериальной крови через систему капилляров гемоглобин в эритроцитах никогда полностью не отдает весь связанный кислород. Обычно в покое артериально-венозная разность не превышает 20 %, а при больших физических нагрузках 30 % [129]. Таким образом, 20-30% эритроцитов, если бы они полностью отдали кислород в ткань, было бы достаточно для нормального функционирования организма, но при кровопотерях этого не происходит. Условия транспорта кислорода после кровопотери не позволяют реализовать его запас. Обратимся к F-углеродам. Жидкие F-углероды, например, F-декалин (ПФД) и F- метилциклогексилпиперидин (ПМЦП) растворяют 40 об.% О2 , F-октилбромид несколько больше, около 50 об.% . Что касается углекислого газа, то по нему вообще лимита нет ( это величина порядка 150-200 об. % ). Кровезамещающая F-углеродная эмульсия, в частности перфторан содержит 20 весовых % F-углеродов, остальное - вода с солевой композицией. И в воде, и в перфторуглеродах растворение/отдача О2 подчиняется линейному закону Генри (рис.10). 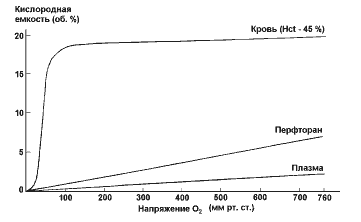
Рис.10 Зависимость кислородной емкости цельной крови, перфторан и плазмы от напряжения О2 в окружающей среде. Нетрудно подсчитать (и это подтверждается прямыми замерами) кислородную емкость эмульсии. На 100 мл воды в перфторане содержится 20 грамм F-углеродов (ПФД+ПМЦП) и 4г поверхностно-активного вещества (ПАВ). Удельный вес F-углеродов около 2г/см3, т.е. 20г частичек эмульсии занимают суммарный объем порядка 10 мл. Если к этой величине прибавить объем ПАВ, то получим суммарный объем порядка 12-14 мл. Остальные 86-88 мл - вода и растворенные в ней соли. Вода растворяет 2-2,4 об.% О2, т.е. в 88 мл воды растворяется 2,1 мл О, а в 12 мл фазы F-углероды+ПАВ растворяется 0,4*12=4,8мл О2. Итого 6,9 мл О2 на 100 мл эмульсии, то есть около 7 об. %. Прямые замеры при давлении 760 мм.рт.ст. и 200С дают эту же величину. Итак мы имеем кислородную емкость для: жидких F-углеродов ~40 об. %; цельной крови ~20 об. %; перфторана ~7 об. %; плазмы, воды и всех традиционных кровезаменителей ~2-2,4 об. % (рис.11). 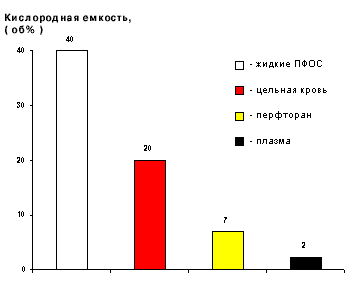
Рис.11 Сравнение кислородной емкости жидких F-углеродов, цельной крови, перфторана (10об% F-углеродной эмульсии) и плазмы крови. Хотя кислородная емкость перфторана по сравнению со всеми традиционными негазотранспортными кровезаменителями (растворы Рингера и Тироде, полиглюкин, желатиноль, плазма крови и т.п.) выше в 3 раза, но приблизительно во столько же раз она ниже кислородной емкости цельной крови. Это казалось бы дает основание говорить о газотранспортной неэффективности перфторана и других F-углеродных эмульсий. Однако при статическом рассмотрении только на основе кислородной емкости упускаются из виду мощнейшие реологические свойства F-углеродных эмульсий. Рассмотрим динамику процесса газообмена в организме. На динамику газообмена влияют три параметра: изменение скорости кровотока, то есть изменения вязкости крови и состояния сосудистого русла; изменение поверхности газообмена; изменение скорости обогащения кислородом крови в легких и скорость его отдачи из крови в тканевую жидкость. Напомним, что все суспензии и эмульсии в той или иной степени являются неньютоновскими жидкостями, а условия их течения в пульсирующем потоках нельзя считать пуазейлевскими [129]. В отличие от гомогенных жидкостей, например, от чистой воды (ньютоновской жидкости), они сжимаются при приложении к ним давления. Находящиеся в жидкости микрочастицы скользят (сдвигаются) относительно друг друга с некоторой скоростью сдвига. Неньютоновские жидкости обладают инерционностью, т.е. начинают течь, если давление становится выше определенной критической величины, а при меньших давлениях ведут себя как упругие тела. Вязкость таких жидкостей определяется размерами, формой и поверхностными свойствами наполняющих их микрочастиц, трением этих частиц друг о друга ( и о стенки сосуда) и скоростью их сдвига [129]. Чем меньше величина вязкости, тем меньше энергозатраты на проталкивание жидкости в сосудах. Вязкость обычно измеряется в Пуазах или Н*с*м-2 (1 Пуаз=0,1 Н*с*м-2). Вязкость перфторана составляет 2,5 сП (сантипуаз), а средняя вязкость крови - 3-7 сП. Вязкость крови зависит от гематокрита (рис.12а), состава (рис.12б) и состояния мембран эритроцитов (рис.12в). 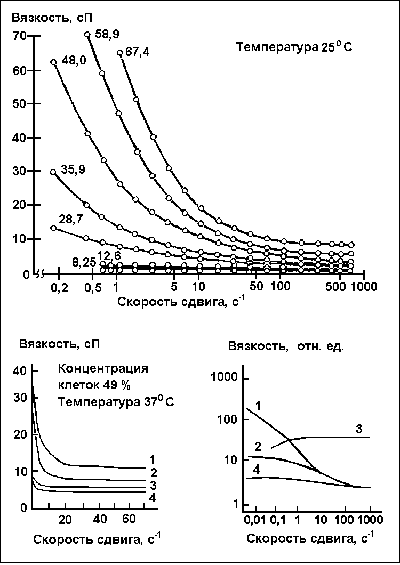
Рис.12 Изменение вязкости от скорости сдвига при различных модификациях крови. Верхний график - вязкость суспензии эритроцитов человека, находящихся в плазме, в которую добавили противосвертывающее средство, при различных значениях концентрации эритроцитов (указаны в % на кривых). Нижние графики: слева - вязкость суспензии цельной крови и ее компонентов (цифры на кривых соответствуют : 1 - глобулин 2,2 вес%, 2 - цельная кровь, 3 - альбумин 3,5 вес%, 4 - фибриноген 0,6 вес%); справа - вязкость суспензии нормальных и модифицированных эритроцитов (цифры на кривых соответствуют: 1- цельная кровь /нормальные эритроциты + плазма/, 2 - нормальные эритроциты в растворе Рингера-Альбумина, 3 - эритроциты, обработанные глютаральдегидом /мембрана изменена, жесткость увеличена/), 4 - эритроциты, обработанные F-углеродом /мембрана изменена, эластичность увеличена/). Вязкость перфторана ниже, чем вязкость цельной крови, поэтому при кровезамещениях вязкость системы "перфторан+оставшаяся кровь" понижается. Тем самым снижается нагрузка на сердце и облегчается кровоток. Кроме того, снижение вязкости связано не только с эффектом разбавления более вязкой жидкости (крови) менее вязкой (перфтораном). При смешении возникает дополнительный нелинейный эффект, определяемый влиянием перфторана на вязкость самой оставшейся после кровопотери крови в связи с модификацией поверхностных свойств эритроцитов - их мембран. Этот эффект связан с растворимостью F-углерода и проксанола в липидах [20, 99, 122]. На рис.12в показан график изменения вязкости крови при разных напряжениях сдвига в зависимости от состояния мембраны эритроцитов. Чем жестче мембрана, тем выше вязкость суспензии. Перфторуглероды, частично растворясь в мембранах эритроцитов, делают их более эластичными, что с одной стороны противодействует повреждающим эритроциты факторам- увеличивает время их "жизни" (до гемолиза), с другой - уменьшает вязкость крови [122]. Таким образом можно ввести интегральный показатель - переноса кислорода по сосудам, например, частное от деления кислородной емкости на вязкость. Он будет характеризовать массоперенос кислорода по сосудистому руслу организма и позволит сравнивать динамические свойства различных газотранспортирующих эмульсий [42]. Однако перенос кислорода по сосудам и уменьшение вязкости крови - это только часть вклада перфторана в газотранспорт. Любопытен тот факт, что в каждый момент времени приблизительно четверть мелких артериол и капилляров либо полностью закрыты, либо кровоток в них резко замедлен [129]. Нервная система путем перекрытия тонких сосудов осуществляет диспетчеризацию потоков крови, а следовательно и кислорода в ткань (особенно в условиях его дефицита при кровепотерях) и уменьшает кровотечение при повреждениях. Однако наряду с положительным эффектом, такая регуляция способствует при массивных кровепотерях развитию шока. Частички F-углерода, размер которых в 100 раз меньше размера эритроцита, могут проникать и в спазмированные микрососуды. При этом улучшается микроциркуляция крови. Особенно важно это в альвеолах легких, т.к. при этом ускоряется обогащение крови кислородом.
Рис.12. Сравнительные размеры эритроцита. Рисунок сделан на основе электронно-микроскопической фотографии (метод криоскалывания). Масштабная шкала (внизу справа) 1 мкм. Средний размер частички в перфторане - 0,07 мкм, а ее поверхность 154*10-4 мкм2. Для сравнения приведем аналогичные средние параметры для эритроцита: диаметр 8,5 мкм, поверхность 156 мкм2 [34]. Нетрудно подсчитать, что в 10 мл эмульсии содержится 5,5*1016 частичек, а их суммарная поверхность в 100 мл перфторана равна 847 м2. С другой стороны в 100 мл крови содержится 4,5* 1011 эритроцитов. Их суммарная поверхность составляет порядка 70 м2 . Таким образом в системе "перфторан + оставшаяся после кровопотери кровь" поверхность газообмена не падает, а напротив возрастает ( 847м2:70м2 ) в 12 раз. На каждый эритроцит приходится свыше 105 частичек эмульсии. Таким образом каждый эритроцит может быть окутан облаком из движущихся в кровотоке частичек F-углерода в 3-4 слоя. Поскольку кислород в F-углеродах растворяется в 20 раз лучше, чем в воде, то такая конденсированная среда вокруг эритроцитов в несколько раз увеличивает эффективную поверхность газообмена. Как уже отмечалось, кислорода в гемоглобине эритроцитов, даже при потери 2/3 эритроцитов, достаточно для функционирования организма, но каждый эритроцит омывается водой. Вода плохо растворяет кислород - лишь 2 об. %. Воду скорее можно назвать экраном, препятствующим транспортировке О2. Таким образом, система передачи кислорода от эритроцита в ткань с коэффициентом полезного действия 2 % в условиях кровопотери может приводить к гипоксии тканей. F-углероды растворяют до 50 об. % кислорода, то есть транспортируют его в 25 раз лучше, чем вода. При замещении части крови перфтораном в кровяносном русле наряду с отдельными эритроцитами движутся и F-углеродные частицы эмульсии. Относительные средние скорости эритроцитов и плазмы неоднократно измерялись in vitro и in vivo [129]. Установлено, что эритроциты движутся в пульсирующем потоке, концентрируясь вблизи оси сосуда. Таким образом эритроцит по отношению к окружающей его жидкости движется с относительной скоростью V: V = (Vэ-Vп) (3), где Vэ - скорость движения эритроцита, Vп - скорость движения F-углеродных частиц. Эритроцит в процессе движения вытесняет находящуюся перед ним воду к стенкам сосуда. Частицы F-углерода, увлекаемые водой, также устремляются к стенка сосуда. Из частичек F- углерода возникают различные динамические структуры. В том числе появляются и структуры типа <жемчужных нитей>, когда частички касаются друг друга и замыкают поверхность эритроцита на стенки сосуда [34]. Такие структуры являются кислородными каналами, т.к. по ним проводимость кислорода в 20-25 раз выше, чем по окружающей их воде. Скорость образования таких структур определяется суммой гидродинамических и диффузионных вкладов и обратно пропорциональна вязкости. Отметим, что образование из частиц эмульсии кислородных каналов важно не только для передачи в ткань кислорода от оставшихся после кровопотери эритроцитов, но и для насыщения этих же эритроцитов кислородом в альвеолах легких при переходе гемоглобина в оксигемоглобин. Таким образом перфторан обеспечивает газотранспорт кислорода из легких в ткань как за счет собственной кислородной емкости, так и за счет своих реологических параметров - низкой вязкости, малых размеров частиц, большой суммарной поверхности, модификации мембран эритроцитов и высокой подвижности F-углеродных частиц в кровотоке при взаимодействии с эритроцитами [45]. Заключение Нашей целью было продемонстрировать прежде всего решение биофизических задач, которые возникали в процессе биомедицинского конструирования F-углеродных газотранспортных эмульсий. На рис.13 приведена обобщенная схема тестирования параметров биологической активности перфторуглеродов, поверхностно-активных веществ и их композиций на биообъектах молекулярно-клеточного уровня (рис.13а) и тестирования характеристик перфторуглеродных эмульсий различного состава на органо-организменном уровне (рис.13б). Такая многоступенчатая схема тестирования использовалась при создании перфторана. С методами синтеза и отбора F-углеродов, помимо статей в сборниках [36-45], можно ознакомиться также в публикациях [87,88,121]. Технология получения F-углеродных эмульсий и обоснование критериев их отбора рассмотрены в работах [22,35,50,52,55,61,63,72,131-134]. Различным аспектам применения F- углеродных соединений в клинике посвящены следующие публикации: для культивирования клеток [23-26], для консервации органов, предназначенных к трансплантации [56,101,102,106,116], для защиты миокарда при операциях на остановленном сердце [46,58,62,80,81,83.98,103,104,107,115,117,119,120], для региональной перфузии конечностей [49,98,135], для поддержания и реабилитации пострадавших с черепно-мозговыми травмами [47,48,59,68,91], для массивных кровезамещений [49,64,70,82,140,141,143], для аппаратов "сердце-легкое" [49,135-139], для улучшения микроциркуляции крови и детоксикационной терапии [53,65,69,75,77,78,142,144,145], а также в других кровесберегающих технологиях [53,54,60,71,73] и для целей офтальмохирургии [66,67,76,146-153]. Следует заметить, что каждый медицинский препарат имеет свои побочные действия и противопоказания. Существует постулат: ubi mel, ibi fel (лат., буквально: где мед, там и яд ). Если утверждается, что противопоказания и побочные эффекты отсутствуют, то это означает, что препарат недоисследован. У всех перфторуглеродных газотранспортных кровезаменителей есть противопоказания и побочные эффекты. Например, у перфторана противопоказания следующие: гемофилия, аллергические заболевания и беременность. Причина к противопоказанию его применения при гемофилии очевидна и вытекает из факта понижения вязкости и увеличения текучести крови. Второе противопоказание - аллергические заболевания - связано с тем, что введение любых микрочастиц в кровоток, даже липидных везикул для парентерального питания, в той или иной степени активирует иммунную систему пациента. Такую же реакцию в большой степени вызывает переливание донорской крови. Хотя F-углеродные молекулы в организме не разлагаются и не метаболизируются, но, образуя сорбционные комплексы с белками и рецепторами клеток, могут затрагивать несколько защитных систем организма. При этом, как уже отмечалось, не исключается возникновение ответов рецепторов клеток ретикуло-эндотелиальной и иммунной систем, перераспределение комплементов в кровяном русле как следствие сорбирования частицами перфторуглерода белков плазмы крови, пространственное перераспределение Т и В лимфоцитов и стимуляция синтеза антител, а также макрофагальная активация и стимуляция детоксицирующей функции печени через образование цитохрома П-450. Чтобы таких реакций у пациентов с нормальной иммунной системой не возникало, при создании перфторана были приняты как композиционные (подбор соответствующих F-углеродов и их пропорций), так и технологические меры (приготовление эмульсий с необходимым размером микрочастиц). Однако у аллергических больных такие реакции неизбежны. При введении тест-дозы перфторана у некотрых пациентов аллергические реакции обостряются, что проявляется в виде покраснения кожи, учащения пульса, уменьшения артериального давления, повышения температуры, появления головной боли или болей за грудиной и в поясничной области, затруднение дыхания, нейропения и даже анафилактические реакции - короче состояние очень похожее на гриппозное. Однако в общем количестве всех пациентов такие люди встречаются редко. Кроме того описанные псевдогриппозные явления как правило самопроизвольно исчезают через 10-15 минут, и происходит смена состояния, отмечаемая пациентами как состояния необычной легкости. Тем не менее при возникновении побочных реакций сразу при введении в кровяное русло первых капель перфторана рекомендуется прекратить его дальнейшее вливание и ввести внутривенно десенсибилизирующие и седактивные препараты в комплексе с кортикостероидными средствами. При повторных введениях перфторана такие реакции не замечаны. Что касается третьего противопоказания - беременность, то эта область с нашей точки зрения пока изучена недостаточно. Перфторуглеродные кровезаменители в допустимых для переливания дозах (20мл/кг) не являются ни тератогенными, ни эмбриотоксичными. Но возможно, что при дозах более 100мл/кг какие-либо тератогенно- эмбриотоксичные эффекты могут проявиться. Кроме того последние исследования на крольчиха показали, что после введения перфторана следы F-углеродов некоторое время обнаруживаются в молоке. Чтобы ответить на вопрос - вредно ли это для крольчат или нет? - требуются дополнительные исследования. В связи с этим введено ограничение на применение перфторана у беременных женщин. Применяя перфторан в экстремальных ситуациях для спасения беременной женщины, врач должен отдавать себе отчет, что не исключен риск нарушения развития плода. Сегодня перфторан продается в аптеках и распространяется по клиническим учреждениям. В городе Пущино Московской области создан банк его запасов на случай чрезвычайных ситуаций Чтобы у читателя не сложилось впечатление, что все работы ведутся только в России, приведем список основнполагающих работ, выполненных в последнее десятилетие и направленных на создание газотранспортных кровезаменителей в других странах [161-212]. Тем не менее на международном рынке в настоящее время других газотранспортных кровезаменителей кроме перфторана нет. Японский кровезаменитель флюозол-DA [161] из- за побочных эффектов с производства снят. Клинические испытания американского препарата оксигент еще не завершины [8]. Хотя F-углеродные кровезаменители выделяют в единый класс инфузионных препаратов, но из изложенного выше материала видно, что каждая F-углеродная среда имеет свои особенности. Ее медико-биологическая эффективность зависит как от композиции F- углеродов и используемого поверхностно-активного вещества, так и от размера частиц эмульсии и технологии ее приготовления. Переносить как достоинства, так и побочные эффекты разных рецептур F-углеродных эмульсий друг на друга нельзя. Вариации F-углеродных и поверхностно-активных композиций открывают возможности для конструирования разнообразных сред для управления жизнедеятельностью клеток, органов и организма, предоставляя широкое поле деятельности в области биомедицинской технологии для специалистов разных профилей. Коллектив был поддержен грантами РФФИ для ведущих научных школ России (96- 15-97851 и 00-15-97985) СПИСОК ЛИТЕРАТУРЫ 1. Иваницкий.Г.Р. / Дар жизни или поцелуй смерти. // Вестник РАН. 1999. Т. 69, ©3. С. 273-276. 2. Иваницкий.Г.Р. / Переливание крови: против, за и альтернатива. // Наука и жизнь. 1999. © 2, С.14-19. 3. Шевченко Ю.Л., Жибурт Е.Б. Безопасное переливание крови. // Изд-во:"Питер". Санкт- Петербург. 2000 4. Константинов Б.А., Рагимов А.А., Дадвани С.А. Трансфузиология в хирургии. // Изд- во:"Аир.Арт."М. 2000 5. Hemoglobin - based blood substitutes: further preclinicals. FDA Reports. Mach 19, 1990. P.19 6. Blood substitutes. // Eds. Chang T.M.S. , Geyer R.P./ N.Y.: Dakker. 1989. 7. Blood substitutes: Preparation, Physlology and Medical Applications. // Eds. Lowe K.C. / Chichester: Ellis Horwood. 1988. 8. Riеss J.G.: / Fluorocarbon - based in vivo Oxygen Transport and Delivery Sysetms. // Vox Sang; Invited Review . Amsterdam. 1991.V.14. P.225-239. 9. Chang T.M.S. / Modified hemoglobin-based blood substitutes: crosslinked, recombinant and encapsulated hemoglobin // Vox Sang.1998. V.74, Suppl.2. P.233-241. 10. Kylstra J.A., Tissing M.O., van der Maen A. // Trans. Am. Soc. Artificial Internal Organs. 1962. V.8. P.378. 1. Clark L.C., Gollan F. /Survival of mammals breathing organic liquids equilibrated with oxygen at atmospheric pressure. // Science. 1966. V.152. ©3730. P.1755-1756. 12. Швирст Э.М., Кринский В.И., Иваницкий Г.Р./ Роль окситаксиса в возникновении диссипативных структур в культуре тетрахимен. // Биофизика. 1984, Т.34. Вып. 4. С. 649-653. 13. Geyer R.P. / Fluorocarbon artificial blood substitutes. / New Engl. J. Med. 1973. V.289. P.1077-1082. 14. Naito R., Yokoyama K../ On the perfluorodecalin - phospholipid emulsion as the red cell substitute./ / Proc. X-th Int. Congr. Nutz-Symp. PFC Artif. Blood. Kyoto. 1975. P. 55-72. 15. Химическая энциклопедия. Изд-во: "Большая Рос.Энциклопедия". М. 1998. Т.5. С.403-410 16. Большая советская энциклопедия. Изд-во: 'Cов. энциклопедия". М. 1978. Т.28. С.113 17. Иваницкий Г.Р., Белоярцев Ф.Ф / О развитии фундаментальных и прикладных исследований в СССР по проблеме "Перфторуглероды в биологии и медицине ".// Препринт. Пущино, 1983, 32 с. (То же самое в сб: [37] С. 9-38) 18. Beloyartsev F.F. et al /Ftorosan - oxygen carrying perfluorochemical plasma subsitute // BSC AS USSR, Pushchino, 1983 19. Lowe K.C./ Perfluorochemicals // Adv. Materials. 1991.V.3.©2. P.70-93. 20. Белоярцев Ф.Ф., Иваницкий Г.Р., Исламов Б.И., Кайдаш А.Н., Маевский Е.И., Макаров К.Н., Михельсон В.А. / Результаты медико-биологической апробации эмульсий перфторуглеродов как кровезаменяющих и перфузионных сред. / / В кн. "Актуальные проблемы производства кровезаменителей, консервантов крови, гормональных и органотерапевтических препаратов", М., 1982, C.17. 21. Голубев А.М., Василъев А.Э., Шибаев Н.В., Маевский Е.И., Исламов Б.И., Склифас А.Н., Аллахвердов Б.Л., Быстрицкий Г.И., Макаров К.Н., Гельфер Ц.М., Овсянникова С.В., Белоярцев Ф.Ф. / Морфологический анализ органов крыс после массивной замены крови эмульсией перфтортрибутиламина. // Архив патологии, 1982, Т. 44, ©11, С. 55-60. 22. Илларионов Э.Ф., Шибаев Н.В., Быстрицкий Г.И., Воробьев С.И., Маевский Е.И., Шипунова Н.А. /Комплексный подход при выборе ПАВ в качестве компонента газопереносящих эмульсий. // В сб. <Актуальные проблемы производства кровезаменителей, консервантов крови, гормональных и органотерапевтических препаратов>, Москва, 1982, С. 70. 23. Иваницкий Г.Р., Архипов В.В., Белоярцев Ф.Ф., Лежнев Э.И. / Культивирование животных клеток на жидких перфторуглеродах. // ДАН, 1981, т. 258, © 1, с. 225-228. 24. Овчинников Ю.А., Иваницкий Г.Р. / Техническая биофизика в развитии биотехнологий.// Вестник АН СССР. 1982, © 7, C. 32-41. 25. Гаврилюк Б.К. , Панкратов С.В., Будницкий А.А., Белоярцев Ф.Ф./ Рост перевиваемых и первичных клеток на жидкой поверхности. // Цитология, 1981, Т.23, © 11, С.1326-1329. 26. Гаврилюк Б.К., Лежнев Э.И., Макарова О.П., Белоярцев Ф.Ф. / Культивирование клеток ВНК-21 на эмульсии жидкого фторуглерода. // Цитология, 1981, Т.24, © 3, С.389-392. 27. Белоярцев Ф.Ф., Иваницкий Г.Р., Исламов Б.И., Шибаев Н.В., Маевский Е.И., Брустовецкий Н.Н. / Замещение больших количеств крови газопереносящей средой на основе эмульсии перфторуглеродов. // ДАН СССР, 1983, Т.270, ©2, С.487-491. 28. Кокоз Ю.М., Кобринский Е.М., Фрейдин Е.М., Исламов Б.И., Маевский Е.И., Белоярцев Ф.Ф., Иваницкий Г.Р. / Действие газопереносящей эмульсии перфторуглеродов на миокард (ионный транспорт, сократительная чувствительность к медиаторам). // ДАН. 1983, Т. 270, © 2, С.459-462. 29. Фрейдин А.А., Кокоз Ю.М., Кобринский Е.М., Маевский Е.И., Илларионов Э.Ф., Быстрицкий Г.И., Белоярцев Ф.Ф., Иваницкий Г.Р. / Влияние неионогенных поверхностно-активных веществ (проксанолов) на натриевые и калиевые токи в миокарде. // ДАН. 1983, Т. 270, © 3, С 728-731. 30. Иваницкий Г.Р. Кто убил профессора Ф.Ф.Белоярцева? История "голубой крови"в калейдоскопе прессы. Изд-во "Вивасват". М.1994 31. Шноль С.Э. Герои и злодеи российской науки. Изд-во 'Крон Пресс". М. 1997. 32. Rich V. / Scandal over Soviet artificial blood research project // Nature. 1988. V.335 ©6186. P.107. 33. Иваницкий Г.Р., Воробьев С.И. / Кровезаменитель "Перфторан".// Вестник РАН. 1997, Т. 67, ©11, С.998-1008. 34. Иваницкий Г.Р., Воробьев С.И. / Организация подвижных структур в кровотоке -основа функционирования перфторуглеродной "искусственной крови ".// Биофизика. 1996, Т. 41, ©1,С.178-190. 35. Воробьев С.И., Иваницкий Г.Р., Мороз В.В., Светлев В.Н., Моисеенко О.М., Лебединская О.В., Ивашина А.И./ Газотранспортные препараты на основе перфторуглеродных эмульсий (обзор). // Вестник интенсивной терапии. 1996. -©2-3.-С.15-21 36. Перфторированные углероды в биологии и медицине. (Под ред. Белоярцев Ф.Ф.) Пущино.1980. 182с. 37. Медико-биологические аспекты применения эмульсий перфторуглеродов. (Под ред. Белоярцев Ф.Ф.) Пущино.1983. 186 с. 38. Фторуглеродные газопереносящие среды. (Под ред. Белоярцев Ф.Ф.) Пущино. 1984. 182 с. 39. Перфторуглероды и медицина. СО АН СССР. Новосибирск. 1990. 154 с. 40. Перфторуглеродные активные среды для медицины и биологии (новые аспекты исследований). (Под ред. Г.Р.Иваницкого, С.И.Воробьева.) Пущино.1993. 242 с. 41. Физико-химические и клинические исследования перфторорганических соединений. (Под ред. Г.Р.Иваницкого, С.И.Воробьева.) Пущино.1994. 120 с. 42. Физиологическая активность фторсодержащих соединений (эксперимент и клиника) (Под ред. С.И.Воробьева И Г.Р.Иваницкого) Пущино.1995. 246 с. 43. Перфторорганические соединения в биологии и медицине ( Под ред. С.И.Воробьева, Г.Р.Иваницкого.) Пущино.1997. 250 с. 44. Физиологически активные вещества на основе перфторуглеродов в военной медицине (Под ред. Г.А.Софронова) Санкт-Петербург. 1997. 157 с. 45. Перфторорганические соединения в биологии и медицине.( Под ред.Г.Р.Иваницкого и В.В.Мороза.) Пущино.1999. 286 с. 46. Исламов Б.И. Противоишемическая защита миокарда эмульсией перфторуглеродов. Автореф дис. докт мед. наук. Ин-т сердечно-сосудистой хирургии им. А.Н. Бакулева АМН СССР. Москва. 1987. 47. Клигуненко Е.Н. Механизмы адаптации к тяжелой травме головного мозга и способы защиты головного мозга от гипоксии. Автореф. дис. докт мед. наук. Институт нейрохирургии им. Н.Н. Бурденко. Москва. 1991. 48. Кривошапкин А.Л. Диагностика обратимости очаговых ишемических нарушений мозгового кровообращения и пути их коррекции (экспериментально-клиническое исследование). Автореф. дис докт. мед. наук. Институт нейрохирургии им. Н.Н. Бурденко. Москва. 1993. 49. Мороз В.В. Пути коррекции гипоксии при клинических состояниях. Автореф. дис докт. мед. наук. Институт хирургии им. А.В. Вишневского. Москва. 1994. 50. Воробьев С.И. Использование субмикронных перфторуглеродных эмульсий, стабилизированных проксанолом, в биологии и медицине. Автореф. дис. докт. биол. наук. Институт медико- биологических проблем МЗ РФ. Москва. 1994. 51. Маевский Е.И.. Коррекция гипоксических систояний путем поддержания функций митохондрий. Автореф. дис. докт. мед. наук. Университет дружбы народов. Москва. 1998. 52. Кузнецова И.Н. Функциональная активность и стабильность эмульсий из перфторуглеродов. Автореф. дис. докт. биол. наук. Рос. НИИ гематологии и трансфузиологии. Санкт- Петербург.1999. 53. Шилов В.В. Детоксикационная терапия острых отравлений липофильными ксенобиотиками с помощью перфторуглеродных соединений. Автореф. дис. докт. мед. наук. Военно-медицинская академия. Санкт-Петербург. 1999. 54. Распутин П.Г. Применение эмульсий перфторорганических соединений в резекционной хирургии печени (экспериментально-клиническое исследование). Автореф. дис. докт. мед. наук. Кировская мед. академия. Киров. 2000. 55. Шибаев Н.В.. Получение и фармакологическая характеристика плазмозаменителя с газотранспортной функцией на основе эмульсии перфторуглеродов. Автореф. дис канд. биол. наук. НИИ по биологическим испытаниям химических соединений. Купавна 1984. 56. Кондуганов Н.Н. Функциональное состояние изолированных почки и сердца животных во время перфузии эмульсий фторуглеродов. Автореф. дис канд. биол. наук. Всесоюзный гематологический научный центр. Москва 1989. 57. Логинова Л.Н. Сравнительная морфологическая оценка действия на органы различных отечественных эмульсий перфторорганических соединений в эксперименте. Автореф. дис канд. биол. наук. Всесоюзный гематологический научный центр. Москва 1989. 58. Воробьев С.И. Создание перфузионной среды с газотранспортной функцией для противоишемической защиты изолированного сердца. Автореф. дис канд. биол. наук. Институт трансплантологии и пересадки органов РАМН. Москва. 1990. 59. Петренко В.Г. Особенности нарушений липидно-перекисного гомеостаза и оптимизация интенсивной терапии у больных в остром периоде тяжелой черепно-мозговой травмы. Автореф. дис. канд. мед. наук. Институт усовершенствования врачей. Харьков. 1990. 60. Панченко С.М. Состояние системы гемокоагуляции после инфузии эмульсии перфторированных органических соединений. Автореф. дис. канд. мед. наук. НИИ гематологии и переливания крови. Ленинград 1990. 61. Беркос М.В. Эмульсии перфторированных соединений и их реактогенность при внутривенном введении в эксперименте. Автореф. дис. канд. мед. наук. НИИ гематологии и переливания крови. Ленинград. 1991. 62. Ладилов Ю.В. Изучение кардиопротекторных свойств эмульсии перфторуглеродов при острой ишемии миокарда. Автореф. дис. канд. биол. наук. Университет дружбы народов. Москва. 1991. 63. Путятина Т.К. Особенности выведения из организма эмульсий перфторорганических соединений, стабилизированных липидами. Автореф. дис. канд. биол. наук. НИИ гематологии и переливания крови. Санкт-Петербург. 1992. 64. Ерошкин И.А. Использование <искусственной крови>, созданной на основе эмульсий перфторорганических соединений, для лечения массивной кровопотери. Автореф. дис. канд. мед. наук. Новосибирский медицинский институт. Новосибирск. 1992. 65. Ломиа, Мераб Исмаил. Экспериментальное применение перфторуглеродного газопереносящего кровезаменителя про ишемии головного мозга. Автореф. дис. канд. мед. наук. НИИ клинической и экспериментальной неврологии им. П.М. Сараджишвили МЗ РГ. Грузия. Тбилиси. 1993. 66. Абу-Аркуб Исмаил. Удаление вывихнутого хрусталика из полости стекловидного тела с помощью жидких перфторорганических соединений (ПФОС). Автореф. дис. канд. мед. наук. Межотраслевой научно-технический комплекс <Микрохирургия глаза>. Москва 1994. 67. Шкворченко Д.О. Комплексное хирургическое лечение отслоек сетчатки, осложненных гигантскими разрывами и отрывами от зубчатой линии с применением перфторорганических соединений. Автореф. дис. канд. мед. наук. Межотраслевой научно-технический комплекс <Микрохирургия глаза>.Москва. 1994. 68. Кривошапкин А.Л. Эффективность инфузий перфторорганических соединений при черепно- мозговой травме в эксперименте. Автореф. дис. канд. мед. наук. Новосибирский медицинский институт. 1995. 69. Литвиненко И.В. Индукторы системы биохимической детоксикации в комплексной терапии рассеянного склероза (экспериментально-клиническое исследование). Автореф. дис. канд. мед. наук. Военно-медицинская академия им. С.М. Кирова. Санкт-Петербург. 1996. 70. Сингаевский А.Б.. Нарушение транспорта кислорода кровью при тяжелой сочетанной травме и его значение для дифференцированной лечебной тактики в постшоковом периоде. Автореф. дис. канд. мед. наук. Военно-медицинская академия им. С.М. Кирова. Санкт-Петербург. 1996. 71. Михайлов С.В. Экспериментально-клиническое обснование возможности сохранения жизнеспособности тканей при огнестрельных переломах. Автореф. дис. канд. мед. наук. Военно- медицинская академия им. С.М. Кирова. Санкт-Петербург. 1996. 72. Капцов В.В. Гомогенизатор высокого давления для приготовления дисперсионных систем медико-биологического назначения. Автореф. дис. канд. тех. наук.. Санкт-Петербургский государственный технический университет. 1996. 73. Тиканадзе А.Д. Применение перфторана при лечении желудочно-кишечных кровотечений язвенной этиологии. Автореф. дис. канд. мед. наук. Военно-медицинская академия им. С.М. Кирова. Санкт-Петербург. 1997. 74. Куликов А.Н. Экспериментальное изучение высокочистых жидких перфторорганических соединений при интравитреальном введении. Автореф. дис. канд. мед. наук. Военно-медицинская академия им. С.М. Кирова. Санкт-Петербург. 1997. 75. Зуев В.В. Эндотоксикоз при острых отравлениях карбофосом и способы его коррекции. Автореф. дис. канд. мед. наук. Военно-медицинская академия им. С.М. Кирова. Санкт-Петербург. 1997. 76. Лебединская О.В. Консервативное лечение травматических гемофтальмов с использованием нового класса перфторорганических соединений - эмульсии перфторана. Автореф. дис канд. мед. наук Межотраслевой научно-технический комплекс <Микрохирургия глаза>. Москва. 1997. 77. Евлашева Н.Н. Оценка эффективности применения перфторорганических соединений в комплексной терапии токсических поражений печени. Автореф. дис. канд. мед. наук. Астраханская государственная медицинская академия. 1997. 78. Язенок А.В. Изменения реологических свойств крови, перекисное окисление липидов при острой лучевой болезни и возможные пути коррекции возникающих нарушений (клинико- экспериментальное исследование). Автореф. дис. канд. мед. наук. Военно-медицинская академия им. С.М. Кирова. Санкт-Петербург. 1998. 79. Чурашов С.В. Экспериментальное обоснование возможности витреального применения высокочистых перфторполиэфиров, перфторпролана и их сочетаний. Автореф. дис. канд. мед. наук Военно-медицинская академия им. С.М. Кирова. Санкт-Петербург. 1998. 80. Судус А.А. Перфтордекалиновая гемопротекция в хирургии открытого сердца. Автореф.дис. канд. мед. наук. Военно-медицинская академия им. С.М. Кирова. Санкт-Петербург. 1998. 81. Цыганков В.К. Острые гастродуоденальные изъязвления слизистой у кардиохирургических больных после оперативного лечения в условиях экстракорпорального кровообращения. Патогенез, профилактика, лечение. Автореф. дис. канд. мед. наук. Военно-медицинская академия им. С.М. Кирова. Санкт-Петербург. 1998. 82. Хоменчук А.И. Применение перфторана в постравматическом и послеоперационном периодах у раненных и больных. Автореф. дис. канд. мед. наук. Государственный институт усовершенствования врачей МО РФ. Москва. 1998. 83. Крюченков Н.Б. Применение перфторана в качестве новой перфузионной среды в клинике ВПС. Автореф. дис. канд. мед. наук. Научный центр сердечно-сосудистой хирургии им. А.Н. Бакулева. Москва. 1998. 84. Склифас А.В. Исследование механизмов аккумуляции и выведения перфтоорганических соединений в организме животных. Автореф. дис.канд. биол. наук. Институт биофизики клетки РАН. Пущино. 2000. 85. Fluorin Chemistry (Ed. J.H.Simons) V.5. / Academic Press. New York, London. 1964. 86. Мацуо М., Отоси С. Соединения фтора // Изд-во "Мир". Москва. 1990. 87. Kabalnov A.S., Makarov K.N., Shchukin E.D. / Stability of perfluoroalkyl halide emulsions. // Colloid and Surface. 1992, V.62, P.101-104. 88. Розенберг Г.Я., Макаров К.Н. / Проблемы создания искусственной крови. // ЖВХО им. Менделеева, 1985, Т.30, С.387-394. 89. Склифас А.Н., Шехтман Д.Г., Образцов В.В., Воробьев С.И., Темнова И.В. / Механизмы распределения и выведения перфторуглеродов при многократных введениях. // Биофизика 1998. Т.43. ©1. С.171-176. 90. Голубев А.М., Ф.Ф.Белоярцев., Васильев А.Э., Покровский А.Э. Реакции биологических систем при замещении крови эмульсиями перфторуглеродов. Изд-во "ТЕИС" М.1993 91. Цыганова В.Г., Попов В.И., Рогачевский В.В., Заргарова Т.А., Туробов Т.А, Иваницкий Г.Р. / Исследование влияния перфторуглеродной эмульсии на клетки центральной нервной системы крыс in vivo и in vitro.// ДАН 2000. Т.375. ©1 (в печати) 92. Белоярцев Ф.Ф., Иваницкий Г.Р., Маевский Е.И., Образцов В.В., Шехтман Д.Г. / Химически инертные фторуглероды - индукторы ферментов монооксигеназной системы микросом печени. // ДАН, 1986, Т.286, ©.3, С.729-732. 93. Образцов В.В., Склифас А.Н., Кукушкин Н.И. / Особенности индукции ферментов монооксидазной системы печени кроликов при внутривенном введении фторуглеродной эмульсии. // Фармакол. и токсикол. 1989. Т.52. ©5. С.60-63. 94. Sklifas A., Obraztov V., Shekhtman D., Gudkova O., Kukushkin N., Makarov. / Acute toxicity of perfluorodecalin emulsion for rabbits. // J. Fluorine Chemictry. 1991. V.54. ©1-3. P.373. 95. Образцов В.В., Шехтман Д.Г., Склифас А.Н., Макаров К.Н. / Взаимодействие перфтороктилбромида с микросомальной монооксигеназной системой печени. // Биохимия, 1993, Т.58, С.1234-1239. 96. Obraztsov V.V., Kabalnov A.S., Makarov K.N., Gross U., Radeck W., Rudiger S. / On the interactions of perfluorochemical emulsions with liver microsomal membranes. // J. Fluor. Chem., 1993. V.63, C.101- 111. 97. Образцов В.В., Тараховский Ю.С., Пономарчук В.В., Склифас А.Н. / Биофизические механизмы токсичности фторуглеродных эмульсий. // Биофизика 1994. Т.39. ©4. С.732-737. 98. Белоярцев Ф.Ф., Кнунянц И.Л., Иваницкий Г.Р, Михельсон В.А., Кайдаш А.Н., Мороз В.В. и др. / Создание и апробация трансфузионных сред - переносчиков кислорода на основе эмульсий фторуглеродов. // Анестезиол. и реаниматол. 1985. -©3.-С. 73 99. Илларионов Э.Ф., Маевский Е.И. / Повышение надежности количественного определения в биологических жидкостях блок-сополимеров типа проксанола и плюроника. // Хим. Фарм. журнал, 1987, ©8. С.1008-1012. 100. Иваницкий Г.Р., Белоярцев Ф.Ф., Исламов Б.И., Онищенко Н.А., Лубяко А.А., Артамонов Г.Д., Грудинова С.В. / Влияние эмульсии перфторуглеродов на защитные свойства кардиоплегических растворов. // Бюлл. экспер. биол. и медицины. 1986, ©8, C.183-185. 101. Онищенко Н.А., Иваницкий Г.Р., Вазагашвили М.О., Маевский Е.И., Жукаускас Г.Ю., Илгявичуте Я.С., Сафронов А.А., Воробьев С.И., Оранская Г.А. / Целесообразность введения фторуглеродной эмульсии в организм трупного донора перед забором почек для трансплантации. // Вестник хирургии. 1989, T.143, © 7, C.94-95. 102. Воробьев С.И., Ладилов Ю.В..Образцов В.В., Иваницкий Г.Р. / Предварительное введение эмульсии перфторуглеродов - новый метод противоишемической защиты миокарда. // Бюлл. эксперимент, биол. и медицины. 1990. © 6, C.19-21. 103. Воробьев С.И., Ладилов Ю.В., Попов Л.А., Баум С.В., Куликова Л.А., Сидоренко В.Г., Шкворченко Д.О., Иваницкий Г.Р. / Влияние химически инертных перфторуглеродных соединений (в составе эмульсий) на первичную активацию амплитуды сердечных сокращений. // Вестник РАМН. 1991, ©6, C.61-64. 104. Ладилов Ю.В.,Исламов Б.И., Воробьев С.И., Иваницкий Г.Р. / Противоишемическое действие перфтоуглеродной эмульсии (ПФУЭ) на миокард собак. // Бюлл. эксперимент. биол. и медицины. 1991, ©2, C.139-142. 105. Ладилов Ю.В.,Исламов Б.И., Воробьев С.И., Иваницкий Г.Р. / Влияние различных доз эмульсии перфторуглеродов на гемодинамику и сократимость ишемического сердца. // Бюлл. эксперимент. биол и медицины. 1992, © 6, C.593-595. 106. Шумаков В.И.,Онищенко Н.А., Саитгареев Р.Ш., Иваницкий Г.Р., Воробьев С.И., Зимин Н.К., Ильинский И.М., Северин В.В., Выборный И.Г., Вавилов П.А., Лапшин А.П. / Применение перфторуглеродной эмульсии при трансплантации легких (экспериментальное исследование). // Биосовместимость. 1993, T.1, ©2, C.57-66. 107. Исламов Б.И. / Фторуглеродная кардиоплегия для защиты миокарда от ишемических повреждений. // Кардиология, 1985, ©12, C.97-100. 108. Исламов Б.И., Ладилов Ю.В., Саксон М.Е., Белоярцев Ф.Ф. / Защитное действие эмульсии фторсоединений от реперфузионных повреждений миокарда // Кардиология, 1986, ©5, C.114- 115. 109. Исламов Б.И. / Сравнительное изучение кардиоплегии эмульсией фторуглеродов и кровью. // Анестезиол. и реаниматол. 1986, ©4, C.17-20. 110. Белоярцев Ф.Ф., Кайдаш А.Н., Исламов Б.И., Маевский Е.И., Кокоз Ю.М., Фрейдин А.А., Образцов В.В. / Оценка возможностей использования фторуглеродной кардиоплегии для противоишемической защиты миокарда. // Вестник АМН СССР, 1986, ©6, C.37-43. 111. Исламов Б.И., Саксон М.Е., Перцов А.М., Фаст А.М., Буевич В.А., Белоярцев Ф.Ф. /. Особенности восстановления электромеханических свойств изолированного миокарда после фторуглеродной кардиоплегии. // Вестник АМН СССР, 1986, ©6, С..43-49. 112. Исламов Б.И. / Противоишемическая защита миокарда при кардиоплегии эмулъсией фторуглеродов. // Грудная хирургия, 1986, N4, C.31-34 113. Исламов Б.И., Маевский Е.И., Воробьев С.И., Кобринский Е.М., Саксон М.Е. / Влияние проксанолов на электромеханическое сопряжение в миокарде и их вклад в защиту от ишемии эмульсиями фторуглеродов. // Вестник АМН СССР, 1987, N2, C.40-45 114. Воробьев С.И., Маевский Е.И., Образцов В.В., Исламов Б.И., Ладилов Ю.В., Баум О.В., Попов Л.А., Сафрошкина А.А., Елецкая С.В./ Кардиотропная и физико-химическая оценка проксанолов. // Хим.-фарм. ж., 1989, N4, C.409-412. 115. Воробьев С.И., Исламов Б.И., Маевский Е.И., Яровая С.М., Телкова Т.Н., Гринева Л.П., Алексеева Г.С., Попова О.Ю., Домбровский В.А./ Влияние онкотических агентов в составе эмулъсии перфторуглеродов на изолированное сердце. // Хим.-фарм. ж., 1989, N1, C.53-56. 116. Воробъев С.И., Исламов Б.И., Ладилов Ю.В. / Возможное применение перфторуглеродной эмульсии для длительного сохранения донорского сердца. // Грудная хирургия, 1990, .N4, C.38- 42. 117. Исламов Б.И., Ладилов Ю.В., Буевич В.А., Бобровский Р.В. / Эмульсия фторуглеродов как средство противоишемической защиты миокарда. // Вестник АМН СССР, 1991, ©3, С.39-43. 118. Воробьев С.И., Васильев А.Э., Исламов Б.И., Кравченко В.А./ Оценка возможности использования эмульсии перфторуглеродов для нормотермической перфузии изолированного сердца. // Патофизиол. и экспер. терапия. 1991, N 6. C.34-36. 119. Ладилов Ю.В., Исламов Б.И., Воробьев С.И. / Влияние поверхностно-активного вещества (ПАВ) проксанола на ишемизированный миокард. // Эксперимент. и клинич. фармакол. 1992, T.55. C.23-25. 120. Воробьев С.И., Ладилов Ю.В., Исламов Б.И., Маевский Е.И., Образцов В.В., Елецкая В.В. / Кардиотропная и физико-химическая оценка блок-сополимеров оксиэтилена и пропилена (проксанола).// Хим. фарм. журнал, 1989. N4, C.78-84. 121. Кнунянц И.Л., Макаров К.Н. Снегирев В.Ф., Гервиц Л.Л., Комарова Л.Ф., Шайдуров В.С., Заболотских В.Ф., Гончаренко А.А., Жирнов О.М., Белоярцев Ф.Ф., Маевский Е.И., Исламов Б.И., Серушкин И.Л., Мухин В.Ю., Бильдинов К.Н. / Перфтор-N-(4-метилциклогексил)- пиперидин как основа газопереносящих перфузионных сред. // Авторское свидетельство © 1094287, приоритет от 30.11.1982, регистрация 22 января 1984. 122. Воробьев С.И., Иваницкий Г.Р., Ладилов Ю.В., Образцов В.В., Склифас А.Н., Понамарчук В.В., Онищенко Н.А. / Модификация мембран клеток перфторуглеродами как возможный механизм уменьшения степени ишемического повреждения миокарда.// ДАН. 1988, T.299, © 1, C.228-230. 123. Иваницкий Г.Р., Крестьева И.Б., Хижняк Е.П, Деев А.А, Руднева О.А. / Самопроизвольная подвижность липидного слоя в системе из трех несмешиваемых жидкостей. // ДАН 2000. Т.374 (в печати) 124. Comparative Animal Physiolodgy (Ed. C.L.Prosser) / W.B. Saunder Com. Philadelphia, London, Toronto. 1973. (есть русский перевод: Сравнительная физиология животных. Под ред. Т.М.Турпаева.Изд-во "Мир".1976. Том 1: Глава: Кислород, дыхание и метаболизм. С.350-429 ) 125. Баев А.А. / Еще раз о "голубой крови"// Вестник Академии наук. 1989.©6. С.55-54. 126. Clark L.C. et al. / Polarographic cerebral oxygen availability, fluorocarbon blood levels efficacy of oxygen transport by emulsions // Biomater., Artif. Cells and Artif. Organs. 1988. V.16. ©103. Р.375- 395. 127. Фуллер Р.А., Розен Дж.Дж. / Материалы для медицины // В мире науки. 1986. ©12. С.57. 128. Иванов К.П./ Современные проблемы дыхательной функции крови и газообмена в легких. // Физиол. журнал им. Сеченова . 1992. Т.78. © 11. С.11-26. 129. Kapo K., Педли Т., Шротер Р., Сид Y.: Механика кровообращения. / Изд-во "Мир" М. 1981. 130. Kabalnov A.S., Makarov K.N., Shcherbakova O.V. / Solubility of fluorocarbons in water as a key parameter determining fluorocarbon emulsion stability. // J. Fluor. Chem. 1990. V.50. P.271-284. 131. Захаров В.Ю., Денисов А.К., Новикова М.Д./ Прямое газофазное каталитическое фторирование неполностью фторированных органических соединений // Ж.Орг. Химии, 1994. Т.30. Вып.12. С.1844-1846. 132. Novikova M., Zakharov V., Denisov A. / Direkt Gas-Phase Fluorination of Hexafluoropropene Trimers //J. Fiuor. Chem. 1992. V.58. P.325. 133. Воробьев С.И., Кутышенко В.П., СклифасА.Н., Сенина Р.Я., Моисеенко О.М., Лебединская О.М., Иваницкий Г.Р. / Комплементактивирующее действие перфторуглеродных эмульсий. // Биосовместимость. 1995, Т.3, © 1-2. С.51-62. 134. Генкин А.М., Глотов Н.А., Маевский Е.И., Ждахина К.С., Колмогорцева В.М., Капралова Л.М./ Влияние хронической интоксикации фтором на окислительные процессы в тканях организма. // Фармакол. и токсикол. 1983. ©3. С.172-177. 135. Мороз В.В., Белоярцев Ф.Ф., Лидии М.П. / Регионарная перфузия конечностей в лечении злокачественных опухолей. // В сб: "Актуальные вопросы клинической онкологии". М. 1982. С. 256-258. 136. Мороз В.В. / Фторуглеродная внелегочная оксигенация как метод интенсивной терапии. // В сб:"Проблемы интенсивной терапии в клинике". М. 1985. С. 121-125 137. Крылов Н.Л., Мороз В.В. / Внелегочная оксигенация, гемосорбция и ультрафильтрация в комплексном лечении тяжелых интоксикаций. // В сб: "Специализированная медицинская помощь и современные проблемы ее интеграции". М. 1986. С. 191-194. 138. Мороз В.В., Бобровский В.В. / Внелегочная фторуглеродная оксигенация. // Анестезиол. и реаниматол. 1996. © 5.С.20-23 139. Miroshnikov A.I., Grishina E.V., Islamov B.I. / The variation in the electrophoretic mobility of erythrocytes after massive blood replacement by "Perftoran" // In. Gell Electrophoresis. (Ed.: W.Schutt, H Klinkmann), Berlin, New York, 1985, P.50-55. 140. Мороз В.В., Крылов Л.Н., Иваницкий Г.Р., Кайдаш А.Н., Онищенко Н.А., Симанов В.А., Воробьев С.И. / Применение перфторана в клинической медицине.// Анестезиол. и реаниматол. 1995. ©6. C.12-17. 141. Крылов Н.Л., Мороз В.В., Белоярцев Ф.Ф. / Применение фторуглеродного кровезаменителя перфторана в клинике. // Воен.-мед. журн. 1985. © 8. С.36-40 142. Крылов Н.Л., Мороз В.В., Ермаченков В.В., Сафонов В.В. / Гемосорбция и инфузия перфторана в комплексном лечении ран и раневой инфекции. // В сб:"Проблемы интенсивной терапии в клинике" М.1985. С.12-13 143. Крылов Н.Л., Мороз В.В. / Перфторан в лечении гипоксии. // В сб: "Опыт Советской медицины в Афганистане". М. 1992. С.30-31 144. Мороз В.В. / Сорбционная терапия у раненых и инфекционных больных в Афганистане. // В сб: "Опыт Советской медицины в Афганистане". М. 1992. С.140-141 145. Хрупкий В.И., Мороз В.В., Писаренко Л.В., Хоменчук А.И./ Использование эмульсии перфторуглеродов в местном лечении ран, осложненных хирургической инфекцией. // Вестник хирургии. 1997. Т.156. © 4.С.53-55. 146. Глинчук Я.И., Сидоренко Д.О., Воробьев С.И., Шкворченко Д.О. / Применение перфторуглеродистых соединений при удалении вывихнутых хрусталиков из полости стекловидного тела. // Офтальмохир. 1991. ©4. С.15-20. 147. Глинчук Я.И., Шкворченко Д.О., Сидоренко В.Г. и др. / Комбинированное лечение отслоек сетчатки, осложненных гигантскими разрывами и отрывами от зубчатой линии с применением ПФОС хир.техника и клинич. результаты. // Офтальмология. 1992. ©4. С.39-44. 148. Глинчук Я.И., Сидоренко В.Г., Каштан О.В., Шкворченко Д.О. / Результаты хирургического лечения неприлегания и рецидивов отслоек сетчатой оболочки, осложненных тяжелой пролиферативной витреоретинопатией. // Офтальмология. 1994. © 2. С.20-25. 149. Глинчук Я.И., Сидоренко В.Г., Каштан О.В. / Лечение отслоек сетчатки с разрывами в заднем полюсе глаза, осложненных пролиферативной витреоретинопатией с применением жидких перфторорганических соединений. // Офтальмохирургия.1994. ©4. С.18-24. 150. Глинчук Я.И., Метаев С.А., Саркисьян А.И. / Клинические результаты применения жидких перфторганических соединений к комплексном хирургическом лечении тракционных отслоек сетчатки с захватом макулярной области при пролиферативной диабетической ретинопатии. // Офтальмология. 1996. © 2. С.7. 151. Глинчук Я.И., Субанбаева З.К., Киселев А.В., Макаров К.Н. / Жидкие перфторорганические соединения нового поколения в хирургическом лечении отечно-геморрагических форм диабетической ретинопатии. // Офтальмология. 1996, ©3. С.8-13. 152. Федоров С.Н., Захаров В.Д., Моисеенко О.М., Лебединская О.В., Тюляев А.П. / Динамика электрофизиологических и ультрасонографических показателей при лечении экспериментального гемофтальма эмульсией перфторан. // Офтальмохирургия. 1995. ©1. С.32- 36. 153. Федоров С.Н., Захаров В.Д., Моисеенко О.М., Средняков В.А., Лебединская О.В., Тюляев А.П., Воробьев С.И./ Опыт использования эмульсии <Перфторан> в лечении различных заболеваний заднего отрезка глаза. // Офтальмохирургия. 1997. ©3. C.3-9. 154. Хлябич Г.Н. и др. / Основные направления разработки и производства кровезаменителей в России. // Росс. мед. журнал. 1997. ©6. С.8. 155. Софронов Г.А., Селиванов Е.А., Ханевич М.Д. / Стратегия поиска искусственных заменителей крови. // Вестн. РАМН. 1999. ©10. С.13-15. 156. Скорик В.И., Судус А.В., Шилов В.В., Жибурт Е.Б., Ващенко В.И., Рождественская Е.Н. / Гемопротекторный эффект перфтордекалина // Бюлл. экспер. биол.и мед. 1996. Т.121. ©5. С.512- 515. 157. Скорик В.И., Шилов В.В., Судус А.В., Зуев В.В. / Использование перфторана для удлинения сроков переносимости острой смертельной гипоксии в эксперименте. // Бюлл. экспер. биол. и мед. 1997. Т.124. ©10. С.477-480. 158. Плужников Н.И., Гусев Д.А. / Иммунологические эффекты перфторана. // Экспер. и клин. фармакология. 1998. Т.61. ©5. С.34-36. 159. Каримов Х.Я., Даминов Ш.Н., Хорошаев В.А. / Влияние перфторана на морфо-функциональное состояние органов пищеварительной системы при экспериментальной язве двенадцатиперстной кишки. // Экспер. и клин. фармакология. 1999. Т.62. ©4. С.33-36. 160. Иноятов Ф.Ш. / Влияние перфторана на параметры биохимической детоксикации у крыс с острым токсическим поражением печени. // Эксперим. и клин. фармакология. 2000. Т.63. ©2. С.67-70. 1. Watanabe M., Ohyanagi H., Saitoh Y. / Experimental study on anaphylactic effects by Fluosol-DA // Jpn. J. Artif. Organs. 1988. V.17. P.1513-1522. 1. Vlahakes G.J., Lee R., Jacobs Jr.E.E., LaRaia P.J., Austen W.G. / Hemodynamic effects and oxygen transport properties of a new blood substitute in a model of massive blood replacement // J. Thorac. Cardiovasc. Surg. 1990. V.100. P.379-388. 1. Simoni J., Feola M., Tran R., Buckner M., Canizaro P.C. / Biocompatibility of hemoglobin solutions. II. The inflammatory reaction of human monocytes and mouse peritoneal macrophages // Artif. Organs. 1990. V.14. P.98-109. 2. Feola M., Simoni J., Tran R., Canizaro P.C. / Nephrotoxicity of hemoglobin solutions // Biomater. Artif. Cells Artif Organs. 1990. V.18. P.233-249. 3. Biro G.P., Anderson P.J., Curtis S.E., Cain S.M. / Stroma-free hemoglobin: its presence in plasma does not improve oxygen supply to the resting hindlimb vascular bed of hemodiluted dogs // Can. J. Physiol. Pharmacol. 1991. V.69. P.1656-1662. 4. Brulisauer M., Bollinger A. / Measurement of different human microvascular dimensions by combination of videomicroscopy with Na-fluoresein (NaF) and indocyanine (ICG) in normals and patients with systemic sclerosis // Int. J. Microcirc. Clin. Exp. 1991. V.10. P.21-31. 5. Moncada S., Palmer R.M.J., Higgs H.A. / Nitric oxide: physiology, patophysiology, and pharmacology.// Pharmacol. Rev. 1991. V.43. P.109-142. 6. Sakaguchi K., Miyauchi Y., Suzuki K., Takahashi A. / Effects of the neo red cell on the blood coagulation system and the complement system // Jpn. J. Artif. Organs. 1991. V.20. P.620- 625. 7. Torres Filho I.P., Intaglietta M. / Microvascular PO2 measurements by phosphorescence decay method // Am. J. Physiol. 1993. V.265. (Heart. Circ. Physiol. 34): P.H.1434-1438. 8. Liard J.F., Kunert M.P. / Hemodynamic changes induced by low blood oxygen affinity in dogs // Am. J. Physiol. 1993. V.264. (Regulatory Integrative Comp. Physio. 33): R396-401. 9. Davies M.G., Hagen P.O. / The vascular endothelium. A new horizon // Ann. Surg. 1993. V.218. P.593- 609 10. Alayash A., Fratantoni J.C., Bonaventura C., Bonaventura J., Bucci E. / Consequences of chemical modification on the free radial reactions of human hemoglobins // Arch. Biochem. Biophys. 1992. V.298. P.114-20. 11. Biro G.P., Ou C., Ryan-McFarlane C. / Oxyradical generation after resuscitation of hemorrhagic shock with blood or stroma-free hemoglobin solution // Artif Cells Blood Substitutes Immobilization Biotechnol. 1995. V.23. P.631-645. 12. Radi R., Beckman J.S., Bush K.M., Freeman B.A. / Peroxynitrite oxidation of sulfhydryls: The cytotoxic potential of superoxide and nitric oxide // J. Biol. Chem. 1991. V.266. P.4244-4250. 13. Balla J., Jacob H.S., Balla G., Nath K., Eaton J.W., Vercellotti G.M. / Endothelial-cell heme uptake from heme proteins: induction of sensitization and desensitization to oxidant damage // Proc. Natl. Acad. Sci. USA. 1993. V.90. P.9285-9289. 14. Motterlini R. Foresti R., Vandegriff K., Intaglietta M., Winslow R.M. / Oxidative-stress in vascular endothelial cells exposed to acellular hemoglobin solutions // Am. J. Physiol. 1995. 269. (Heart. Circ. Physiol. 38): H648-655. 15. Ogata Y., Okamoto T., Suzuki K., Kamitani T. / The development of the Neo Red Cells (NRC) with enzymatic reduction system of the methemoglobin // Artif. Blood. 1994. V.2. P.62-66. 16. McGown E.L., Lyons M.F., Marini M.A., Zegna A. / Reduction of extracellular methemoglobin by erythrocytes // Biochem. Biophys. Acta. 1990. V. 1036. P. 202-206. 17. Suematsu M., Kashiwagi S., Sano T., Goda N., Shinoda Y., Isnimura Y. / Carbonmonoxide as an endogenous modulator of hepatic vascular perfusion // Biochem. Biophys. Res. Commun. 1994. V.205. P.1333-1337. 18. Ogata Y., Okamoto T., Suzuki K., Kamitani T. / The development of neo red cells (NRC) with enzymatic reduction system of the methemoglobin // Artif. Blood. 1994. V.2. P.62-66. 19. Laing R.B.S., Milne L.J.R., Leen C.L.S., Malcom G.P., Steers A.J.W. / Anaphylactic reactions to liposomal amphotericin // Lanset 1994. V.344. P.682. 20. Szebeni J., Wassef N.M., Spielberg H., Rudolph A.S., Alving C.R. / Complement activation in rats by liposomes and liposome-encapsulated hemoglobin: evidence for anti-lipid antibodies and alternative pathway activation // Biochem. Biophys. Res. Commun. 1994. V.205. P.255-263. 21. Rabinovici R., Rudolph A.S., Vernick J., Feuerstein G. / Lyophylized liposome encapsulated hemoglobin: evaluation of hemodynamic, biochemical, and hematologic responses // Crit. Care. Med. 1994. V.222. P.480-485. 22. Kerger H., Torres Filho I.P., Rivas M., Minslow R.M., Intaglietta M. / Systemic and subcutaneous microvascular oxygen tension in conscious Syrian golden hamsters // Am. J. Physiol. 1995. 2671. (Heart. Circ. Physiol. 37): P.H.802-810. 23. Tsai A.G., Friensenecker B., Sakai H., Kerger H., Intaglietta M. / The mechanism of tissue oxygenation and the design of oxygen carrying plasma expanders // In: Advances in blood substitutes: industrial opportunities and medical challenges. (Ed. by Winslow R.M., Vandegriff K., Intaglietta M.) Birkhauser, Boston. 1995. P.189-206. 24. Lee R., Neya K., Svizzero A., Vlahakes G.J. / Limitations of the efficacy of hemoglobin-baased oxygen carrying solutions // J. Appl. Physiol. 1995. V.79. P.236-242. 25. Sprung J., Mackenzie C.F., Barnas G.M., Williams J.E., Parr M., Christenson R.H., Hoff B.H., Sakamoto R., Kramer A., Lottes M. / Oxygen transport and cardiovascular effect of resuscitation from severe hemorrhagic shock using hemoglobin solution. Crit Care Med. 1995. V.23. P.1540-1553. 26. Pries A.A., Heide J., Ley K., Klotz K-F., Gaehtgens P. / Effect of oxygen tension on regulation of arteriolar diameter in skeletal muscle in situ // Microvasc. Rec. 1995. V.49. P.289-299. 27. Johnson P.C., Richmond K., Shonat R.D., Toth A., Pal M., Tischler M.E., Lynch R.M. / Oxygen delivery regulation: implication for blood substitutes // In Blood Substitutes: Physiological Basis of Efficacy (Ed. by Winslow R.M., Vandegriff K.D., Intaglietta M.) Birkhauser, Boston, 1995. P.175-186. 28. Ellsworth M.L., Forrester T., Ellis C.G., Dietrich H.H. / The erythrocyte as a regulator of vascular tone // Am. J. Physiol. 1995. V.269 (Heart. Circ. Physiol. 38): H2155-2161. 29. Kasa W., Roth R. / Activation of complement by human hemoglobin and by mixtures of hemoglobin and endotoxin // Biochem. Biophys. 1995. V.1245. P.49-56. 30. Leech C.J., Faber J.E. / Differential sensitivity of venular and arteriolar alpha-adrenergic receptor constriction to inhibition by hypoxia: role of receptor subtype and coupling heterogeneity. // Circ. Res. 1996. V. 78. 1064-1074. 31. Intaglietta M., Johnson P.C., Winslow R.M. / Microvascular and tissue oxygen distribution // Cardiovasc. Res. 1996. V.32. P.632-643. 32. Sakai H., Tsuchida E. / Physiological roles of messenger molecules (NO, CO). // Chemistry. 1996. V.51. P.62-63. 33. Harder D.R., Narayaran J., Birks E.K., Francois Liard J., Imig J.D., Lombard J.H., Lange A.R., Roman R.J. / Identification of a putative microvascular oxygen sensor. // Circ. Res. 1996. V.79. P.54-61. 34. Vandegriff K.D., Winslow R.M. / A theoretical analysis of oxygen transport: A new strategy for the design of hemoglobin-based red cell substitutes // In Blood Substitutes: New Challenges (Ed. by Winslow R.M., Vandegriff K.D., Intaglietta M.) Birkhauser, Boston, 1996. P.124-131. 35. Kunert M.P., Liard J.F., Abraham D.J., Lombard J.H. / Low-affinity hemoglobin increases tissue PO2 and decreases arteriolar Diameter and flow in the rat cremaster muscle // Microvasc. Res. 1996. V.52. P.58-68. 36. Szebeni J., Wassef N.M., Rudolph A.S., Alving C.R. / Complement activation in human serum by liposome-encapsulated hemoglobin: the role of natural anti-phospholipid antibodies // Biochem. Biophys. Acta. 1996. V.1285. P.127-130. 37. Abudullah F., Whiteford M., Ovadia P., Neville L.F., Rudolph A.S., Grillo S., Rabinovici R. / Effect of liposome encapsulated hemoglobin on serum triglyceride, total cholesterol, LDL and HDL cholesterol measurements // Lipids. 1997. V. 32. P. 377-382. 38. Rudolph A.S., Sulpizio A., Hieble P., MacDonald V., Chavez M., Feuerstein G. / Liposome encapsulation attenuates hemoglobin-induced vasoconstriction in rabbit arterial segments // J. Appl. Physiol. 1997. V.82. P.1826-1835. 39. Fagrell B., Intaglietta M. / Microcirculation: its significance in clinical and molecular medicine // J. Intern. Med. 1997. V.241. P.349-362. 40. Intaglietta M. / Whitaker Lecture 1996: microcirculation, biomedical engineering, and artificial blood // Ann. Biomed. Eng. 1997. V.25. P.593-603. 41. Chu D., Oglivy C.S. / Isovolemic hemodilution with purified and polymerised bovine hemoglobin in a rabbit model of focal cerebral ischemia. // Chinese J. Physiol. 1997. V.40. P.63-69. 42. Fenger-Gron J., Mulvany M.J., Christensen K.L. / Intestinal Blood flow is controlled by both feed arteries and microcirculatory resistance vessels in freely moving rats // J. Physiol. Lond. 1997. V. 498. P. 215-224. 43. Kerger H., Tsai A.G., Saltzman D.J., Winslow R.M., Intaglietta M. / Fluid Resuscitation with O2 vs. Non-O2 carriers after 2 h of hemorrhagic shock in conscious hamsters // Am. J. Physiol. 1997. (Heart. Circ. Physiol 41):PH525-537. 44. Collman J.P., Herrmann P.C., Fu L., Eberspancher T.A., Eubanks M., Boitrel B., Hayoz P., Zhang X., Brauman J.I., Day V.W. / Aza-crowncapped porphyrin modelled of myoglobin: steadies of the steric interactions of gas binding // J. Am. Chem. Soc. 1997. V.119. P.3481-3489. 45. Tsai A.G., Friesenecker B., McCarthy M., Sakai H., Intaglietta M. / Increased viscosity during extreme isovolemic hemodilution lowers vascular resistance // Ann. Biomed. End. 1997. V. 25. P. S-14. 46. Phillips W.T., Klipper R., Frense D., Rudolph A.S., Javors M., Goins B. / Platelet reactivity with liposome- encapsulated hemoglobin in rat // Exp. Hematol. 1997. V.25. P.1347-1356. 47. D'Angillo F., Chang T.M.S. / Reduction of hydroxyl radial generation in a rat hindlimb model of ischemia-reperfusion injury using crosslinked hemoglobin-superoxide dismutase-catalase // Artif. Cells Blood Substitute Immobilization Biotechnol. 1997. V. 25. P. 163-180. 48. Szebeni J., Wassef N.M., Hartman K.R., Rudolph A.S., Alving C.R. / Complement activation in vitro by the red cell substitute, liposome-encapsulated hemoglobin: mechanism of activation and inhibition by soluble complement receptor type I // Transfusion. 1997. V.37. P.150-159. 49. Sakai H., Tsai A.G., Kerger H., Park S.I., Takeoka S., Nishide H., Tsuchida E., Intaglietta M. / Subcutaneous microvascular responses to hemodilution with a red cell substitutes consisting of polyethyleneglycol-modified vesicles encapsulating hemoglobin // J. Biomed. Mater. Res. 1998. V.40. P.66-78. 50. Goda N., Suzuki K., Naito M., Takeoka S., Tsuchida E., Ishimura Y., Tamatani T. / Distribution of oxygenase isoforms in rat liver. Topographic basis for carbon monoxide-mediated microvascular relaxation // J. Clin. Invest. 1998. V.101. P.604-612. |
||||||||||||||||||||||||||||||||||||||
| Размещение рекламы | |
|
| |

 Articles
Articles